Ацетилбензоил
Cтраница 3
Совершенно различное влияние на ход процесса оказывают уксусная и бензойная кислоты. Уксусная кислота способствует снижению выхода перекиси ацетилбензоила и максимальной скорости ее накопления, увеличению выхода смол и других продуктов. [31]
Вторым процессом, по которому этильные радикалы могут расходоваться без образования газообразных углеводородов, является этилиро-вание бензольного ядра ацильных перекисей. При взаимодействии тетраэтилолова с перекисями бензоила и ацетилбензоила этот процесс имеет лишь побочный характер. [32]
Это подтверждается низким выходом СО2, особенно в реакции с перекисью ацетилбензоила, для которой, как уже говорилось, при свободно-радикальных процессах реакция 18 является обязательной. [33]
Диацилперекиси могут применяться в синтезе органических соединений. Как показали Ю. А. Ольдекоп и Р. В. Кабердин 278, при распаде перекисей ацетила и ацетилбензоила в 1 1 2 2-тетра-хлорэтане образуются димерные ( CbCHCCbCClgCHCb), тример-ные и более высокополимерные вещества; в присутствии диалкил-перекисей, в отличие от диацилперекисей, эта реакция не протекает. [34]
Установлено, что при неинициированной полимеризации хлортрифторэтилена индукционный период обусловлен присутствием О2, причем продолжительность индукционного периода обратно пропорциональна произведению концентрации О2 и мономера. Полимеризация в этом случае инициируется образующимися продуктами окисления подобно параллельно испытанной перекиси ацетилбензоила. Энергия активации реакции составляет 9 ккал / моль. [35]
Диацилперекиси могут применяться в синтезе органических соединений. Как показали Ю. А. Ольдекоп и Р. В. Кабердин 278, при распаде перекисей ацетила и ацетилбензоила в 1 1 2 2-тетра-хлорэтане образуются димерные ( С СНССЬСС СНСЬ), тример-ные и более высокополимерные вещества; в присутствии диалкил-перекисей, в отличие от диацилперекисей, эта реакция не протекает. [36]
Исследование показало, что гекса-этилдигерман и гексаэтилдисилан не реагируют с перекисями бен-зоила, ацетилбензоила и грет-бутила при комнатной температуре. [37]
Исследование показало, что гекса-этилдигерман и гексаэтилдисилан не реагируют с перекисями бен-зоила, ацетилбензоила и трег-бутила при комнатной температуре. [38]
На рис. 1 приведены кинетические кривые расходования альдегида и накопления перекиси ацетилбензоила и надбензойной кислоты. Как видно из рисунка, основным продуктом реакции при окислении бензальдегида в уксусном ангидриде является перекись ацетилбензоила. Кинетическая кривая ее накопления носит типичный S-образный характер. [39]
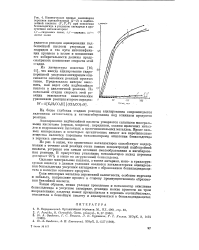 |
Кинетические кривые накопления перекиси ацетилбензоила ( 1 - 3 и надбен-зойной кислоты ( Г, 2, 3 при окислении бензальдегида в уксусном ангидриде в присутствии катализаторов. [40] |
Ацилирование надбензойной кислоты ускоряется сильными минеральными кислотами ( серная, хлорная), пиридином, солями щелочных металлов и гидроокисями щелочных и щелочноземельных металлов. Кроме сильных минеральных и некоторых органических кислот все перечисленные вещества являются хорошими катализаторами окисления бензальдегида в перекись ацетилбензоила. [41]
Более четко влияние отдельных продуктов реакции на ход процесса удалось выявить в случае замены части уксусного ангидрида на бензол. Из рисунка видно, что бензойная кислота и перекись бензоила способствуют повышению выхода пере-кисных соединений, в то время как перекись ацетилбензоила и уксусная кислота снижают его. Интересно влияние добавок инициаторов по ходу процесса. [42]
Особенно многообразно действие перекисных катализаторов типа перекиси бензоила ( CeHs СОЬСЬ, применение которых очень распространено. Большой выбор катализаторов дает возможность регулировать процесс полимеризации. Например, перекись бензоила или ацетилбензоила легко приводит у органических виниловых эфиров к веществам с ограниченной набухае-мостыо, а при перекисях более высокомолекулярных соединений характерно образование полимеров с прекрасной растворимостью. [43]
Сначала жидкость становится красной и мутится, затем начинается сильное выделение газа и пены. Когда выделение газа прекратится и пена собьется в липкую черную смолу, прилипающую к стенкам сосуда, жидкость фильтруют и фильтрат подкисляют уксусной кислотой. При этом тотчас же выпадает кристаллический сырой монооксим ацетилбензоила, который очищают перекристаллизацией из метилового алкоголя с животным углем. При нагревании с разбавленной серной кислотой оксим легко распадается с почти теоретичесгаш выходом на дикетон и гидроксил-амин. На 4гоксима берут 60 сл 3 10 % - ной серной кислоты. Ацетилбепзоил представляет собою легколетучее с водяным паром тсмнижелтое масло, тяжелее воды, которое обладает характерным сладковатым и в то же время напоминающим хинон острым запахом. [44]
Перекись бензоила, наряду с сокращением индукционного периода, приводит к некоторому повышению максимальной скорости накопления и выхода перекиси ацетилбензоила. Добавки надбензоиной кислоты, сокращая начальный период, вызывают значительное торможение на более глубоких стадиях. Этим и объясняются высокие требования к чистоте исходного бензальдегида, поскольку в противном случае нельзя достичь воспроизводимых и стабильных результатов. Добавки перекиси ацетилбензоила и особенно надбензоиной кислоты ускоряют процессы уплотнения и приводят тем самым к более высокому содержанию смол в конечном продукте. [45]
Страницы: 1 2 3 4