Молекула - пиррол
Cтраница 3
Введение кислотного радиола, подобно введению и других отрицательных групп вроде ацильных остатков, придаст молекуле пиррола большую устойчивость. Так пнрролкарбоно-вые кислоты, прежде всего их эфиры, представляют из себя, обыкновенно, хорошо кристаллизую. [31]
Пиррол с большинством диенофилов обычно реагирует лишь по схеме заместительного присоединения, которое направляется в а-положения молекулы пиррола и осложняется побочно протекающей сополимеризацией. Образующиеся при заместительном присоединении вещества могут быть использованы для дальнейших синтезов. [32]
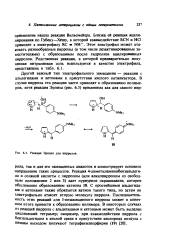 |
Реакция Эрлнха для пнрролов. [33] |
С простейшими альдегидами н кетонами также образуется катион такого типа, но затем он злектрофильно атакует вторую молекулу пиррола. Последовательность этих реакций для 5-незамещенного пиррола может в конечном итоге привести к образованию полимера. [34]
Рентгенографические [19] и микроволновые [20 21] исследования структуры пиррола, а также изучение комбинационных и инфракрасных спектров приводят к заключению, что молекула пиррола должна быть плоской и принадлежать к точечной группе С2, что служит основой определения системы постоянных потенциальной энергии для выяснения некоторых особенностей силового поля молекулы и расчета частот нормальных колебаний пиррола и его дейтерозамещенных для обоснования интерпретации колебательных спектров. [35]
Если в качестве электролита используются перхлорат тетрабутиламмония, то возникает легированный полимер, в котором на один ион перхлората приходятся три молекулы пиррола. [36]
Так, 1-метилпиррол ( 1) конденсируется с диметиловым эфиром аце-тилендикарбоновой кислоты, образуя аддукт ( III), содержащий одну молекулу пиррола на две молекулы эфира. [37]
Из ИК-спектров и большого числа других физических методов следует, что кроме уже обсуждавшихся эффектов существует и такая водородная связь между молекулами пиррола, при которой NH-rpynna одной молекулы взаимодействует с я-электронной системой другой молекулы. [38]
Особая устойчивость ароматического цикла тиофена связана, вероятно, главным образом с более полным выравниванием я-электрон-ной плотности в молекуле тиофена по сравнению с молекулами пиррола и фурана, поскольку в данном случае в делокализации возможно участие of - орбиталей атома серы. [39]
В конце XIX столетия польские ученые Ненцкий и Мархлевский установили, что в составе хлорофилла, так же как и в гемоглобине, центральное место занимает порфириновое кольцо, построенное из четырех молекул пиррола, соединенных мостиками из СН групп; в центральной полости всей структуры помещается магний, так же как в гемоглобине железо. [40]
Таким образом, имеется возможность поставить в соответствие каждую частоту колебательного спектра пиррола ( или две частоты вследствие снятия вырождения для типов симметрии Ег и Ez) определенной частоте в спектре бензола, что представлено в табл. 2.2 Для соответствующих частот молекул пиррола и бензола должны быть общими основные характерные черты форм колебаний. [41]
Образование водородной связи между атомом N и ОН-группой поверхности при адсорбции приводит к смещению электронной плотности свободной пары электронов обратно к атому N. В молекуле пиррола, в которой свободная пара электронов азота участвует в образовании устойчивого электронного секстета молекулы, адсорбция не приводит к локализации свободной пары электронов у атома N и сильного понижения частоты N - Н не происходит. [42]
Известно, что причиной повышения значения постоянных такого рода является увеличение кратности смежных связей С-С. Однако в случае молекулы пиррола очевидно, что по сравнению с этиленом кратность связей С-С не может быть выше. Можно предположить, обобщая расчеты силовых постоянных для других молекул, что второй причиной повышения значения этих силовых постоянных является наличие напряжения в цикле. По-видимому для пиррола свойственно именно значительное напряжение цикла, что желательно исследовать другими физико-химическими: методами. [43]
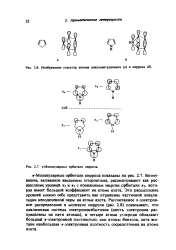 |
Изображение структур аниона циклопеитадиеинла ( а и пиррола ( 6. [44] |
Рассчитанное т-электрон-ное распределение в молекуле пиррола ( рис. 2.8) показывает, что циклическая система электроноизбыточна ( шесть электронов распределены на пяти атомах), и четыре атома углерода обладают большей т-электронной плотностью, чем атомы бензола, хотя все-таки наибольшая т-электронная плотность сосредоточена на атоме азота. [45]
Страницы: 1 2 3 4