Кислое мыло
Cтраница 1
Кислое мыло представляет собой сложную смесь мыла и жир. [1]
Кислые мыла нерастворимы в воде и легко отделяются от водного раствора бикарбоната натрия. Под действием двойного растворителя, состоящего из водного этилового спирта и легкого бензина, кислое мыло разрушается, при этом в бензин переходят только свободные жирные кислоты, а соли остаются в спирто-водном растворе. [2]
Кислые мыла ненасыщенных жирных кислот при повышенной температуре в мыльных растворах частично растворяются. [3]
Так называемые кислые мыла представляют собой средние соли жирной кислоты в соединении с различными количествами свободной жирной кислоты. [4]
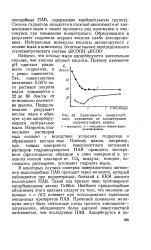 |
Зависимость поверхностного натяжения от концентрации лаурилсульфата натрия. [5] |
Найдено, что кислые мыла адсорбируются значительно сильнее, чем анионы жирной кислоты. Поэтому изменение рН сдвигает равновесие гидролиза, и зин / см а резко изменяется. Так, поверхностное натяжение 0 05 % - но-го раствора лаурата калия повышается с 22 до 60 дин / см от ничтожного количества щелочи. Подщела-чивание разрушает кислое мыло и образует хуже адсорбирующееся нейтральное мыло. Напротив, под-кисление растворов мыл снижает а вследствие усиления гидролиза и образования кислых мыл. Поэтому важно, например, при точных измерениях поверхностного натяжения растворов гидролизующихся ПАВ проводить эксперимент ( приготовление образцов и сами измерения) в условиях полной изоляции от СО2 воздуха, которая, поглощаясь растворами, усиливает гидролиз мыла. [6]
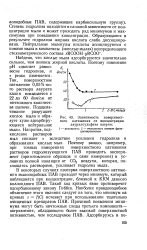 |
Зависимость поверхностного натяжения от концентрации лаурилсульфата натрия. [7] |
Найдено, что кислые мыла адсорбируются значительно сильнее, чем анионы жирной кислоты. Поэтому изменение рН сдвигает равновесие гидролиза, и ин / см о резко изменяется. Так, поверхностное натяжение 0 05 % - но-го раствора лаурата калия повышается с 22 до 60 дин / см от ничтожного количества щелочи. Подщела-чивание разрушает кислое мыло и образует хуже адсорбирующееся нейтральное мыло. Напротив, под-кисление растворов мыл снижает а вследствие усиления гидролиза и образования кислых мыл. Поэтому важно, например, при точных измерениях поверхностного натяжения растворов гидролизующихся ПАВ проводить эксперимент ( приготовление образцов и сами измерения) в условиях полной изоляции от СО2 воздуха, которая, поглощаясь растворами, усиливает гидролиз мыла. [8]
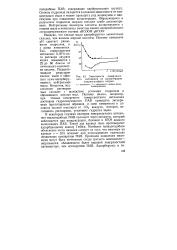 |
Зависимость поверхностного натяжения от концентрации лаурилсульфата натрия. [9] |
Найдено, что кислые мыла адсорбируются значительно сильнее, чем анионы жирной кислоты. Поэтому изменение рН сдвигает равновесие гидролиза, и о резко изменяется. Так, поверхностное натяжение 0 05 % - но-го раствора лаурата калия повышается с 22 до 60 дин / см от ничтожного количества щелочи. Подщела-чивание разрушает кислое мыло и образует хуже адсорбирующееся нейтральное мыло. Напротив, под-кисление растворов мыл снижает а вследствие усиления гидролиза и образования кислых мыл. Поэтому важно, например, при точных измерениях поверхностного натяжения растворов гидролизующихся ПАВ проводить эксперимент ( приготовление образцов и сами измерения) в условиях полной изоляции от СО2 воздуха, которая, поглощаясь растворами, усиливает гидролиз мыла. [10]
Для предупреждения образования кислого мыла необходимо при нейтрализации всегда иметь в мыльной массе избыток свободной едкой щелочи ( не ниже 0 1 %) и одновременно достаточную концентрацию соли. В этих же целях загрузку жирных кислот производят в раствор щелочи, а не наоборот. [11]
Это явление напоминает способность к растворению кислых мыл в холодной воде, но с той, однако, разницей, что здесь характер этой способности диаметрально противоположен, ибо в данном случае, чем короче алкильная цепь, тем выше растворимость мыла в воде. [12]
Изучен процесс экстракции свободных кислот из водио-спиртового раствора кислого мыла бензином. [13]
ККМ мыл жирных кислот почти идентично, образование же кислого мыла, например при избытке жирной кислоты или при уменьшении рН добавкой неорганической кислоты, приводит к заметному снижению ККМ и увеличению солюбилизирующей способности. [14]
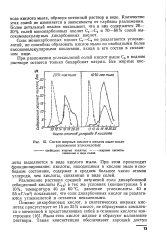 |
Состав жирных кислот в кислом мыле после разложения углекислотой. [15] |
Страницы: 1 2 3 4