Потеря - кристаллизационная вода
Cтраница 2
В области температур 256 - 636 С наблюдается ряд эндоэффектов, связанных с потерей межрешеточной и кристаллизационной воды. Порошок, полученный в условиях плазмы, практически не содержит кристаллизационной влаги и дает незначительный эндоэффект. [16]
Эндотермический эффект при 57 С связан с плавлением кристаллогидрата, а эффект при 256 С - с потерей кристаллизационной воды вследствие испарения. Это подтверждается тем, что оба эндотермических эффекта отсутствуют на термограмме безводного перхлората кальция. Это предположение подтверждается тем, что перхлорат кальция при 340 С остается твердым и не показывает еще никаких признаков плавления или разложения. [17]
Кристаллы железо-аммонийных квасцов должны быть светло-фиолетового цвета, если же они обесцвечены, то это говорит о потере кристаллизационной воды. [18]
Фазовые превращения гидратов мыл могут существенно отличаться от фазовых превращений безводных мыл и, в отдельных случаях, могут вызываться потерей кристаллизационной воды. [19]
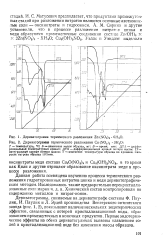 |
Дериватограмма термического разложения Zn ( NO3 2 6Н2О. [ IMAGE ] Дериватограмма термического разложения Си ( NO3. 2 ЗН2О. [20] |
Эрдей производства Венгерского оптического завода ( рис. 1, 2), показывают наличие нескольких эндотермических эффектов, связаннных с потерей кристаллизационной воды, образованием промежуточных и конечных продуктов. Первые эндотермические эффекты на обеих дериватограммах вызваны плавлением солей в кристаллизационной воде без изменения массы образцов. [21]
 |
Термограмма препарата АФС, высушенного без нагревания. / - дифференциальная кривая нагревания. 2 - потери массы. [22] |
Термограмма исходного препарата АФС ( рис. 8) имеет два эндотермических эффекта: первый - при 140 С, соответствующий потере кристаллизационной воды, и второй - при 240 С, соответствующий потере части конституционной воды. При наблюдении под микроскопом установлено, что при 140 - 150 С появляется новая фаза, которая при 170 С составляет основную массу продукта. [23]
При взаимодействии мочевины с дигмдратом дикаль-цийфосфата СаНРО4 - 2Н2О не получается комплекса, подобного CaSC4 4СО ( N1 2) 2 - Мочевина лишь ускоряет потерю кристаллизационной воды из дикальций-фосфата. [24]
Кроме того, вопреки распространенному мнению, ткань из длинноволокнистого хризотилового асбеста при нагревании в течение продолжительного времени при 1093 ЭС, в результате которого происходит потеря кристаллизационной воды и изменение структуры ( превращение в кристаллический хризотил), сохраняет форму ( рис. 69) и относительно высокую долю полезной механической прочности. [25]
При термическом разложении кристаллогидрата Na2SO3S - 5H2O в контролируемых условиях возможно образование сульфата натрия, сероводорода и воды, либо вначале ( до 100 С) происходит потеря кристаллизационной воды, а затем ( выше 220 С) превращение в сульфат натрия и пентасуль-фид ( 2 -) натрия, который неустойчив и при дальнейшем прокаливании разлагается до сульфида натрия и серы. Составьте уравнения всех параллельно идущих реакций, а также суммарное уравнение реакции термического разложения исходного кристаллогидрата. Предложите способы разделения и обнаружения всех продуктов. [26]
Запасной стандартный раствор железа приготовляется из железокалиевых квасцов [ Fe2 ( SO4) 3 - K2SO4 - 24H2O ] или железо-аммонийных квасцов FeNH4 ( SO4) 2 - 12H2O ], которые должны быть светло-фиолетового цвета, но не бесцветные, так как последнее указывает на потерю кристаллизационной воды. Отвешивают точно 0 4505 г железокалиевых квасцов или 0 4317 железоаммо-нийных квасцов и растворяют в небольшом количестве дистиллированной воды в мерной колбе объемом в 500 мл. После растворения добавляют 3 мл концентрированного раствора НС1 и доводят объем до метки. Fe и является основным стандартным раствором. [27]
Результаты термогравиметрического исследования оксиэти-лидендифосфонатов показывают, что все они являются кристаллогидратами. Потеря кристаллизационной воды для тетразамещенных комплексов начинается уже при 30 - 40 С. Одностадийное удаление воды характерно для кристаллогидратов дизамещенных оксиэтилидендифос-фонатов Mg и Са, причем для последнего характерна чрезвычайно высокая термическая устойчивость: его дегидратация начинается при 173 С. [28]
Результаты термогравиметрического исследования оксиэти-лидендифосфонатов показывают, что все они являются кристаллогидратами. Потеря кристаллизационной воды для тетразамещенных комплексов начинается уже при 30 - 40 С. Одностадийное удаление воды характерно для кристаллогидратов дизамещенных оксиэтилидендифос-фонатов Mg и Са, причем для последнего характерна чрезвычайно высокая термическая устойчивость: его дегидратация начинается при 173 С. [29]
Помещают в сухую пробирку небольшое количество полученного продукта и осторожно нагревают. Происходит потеря кристаллизационной воды, сопровождающаяся изменением цвета. [30]
Страницы: 1 2 3 4