Скорость - коррозия - железо
Cтраница 4
Большинство приборов рассчитано на измерение скорости коррозии железа. Если используются электроды из других металлов, то показания прибора пересчитываются умножением на коэффициенты, приводимые в паспортах на оборудование. [46]
При повышении концентрации кислорода в воде скорость коррозии железа сначала увеличивается, достигая максимального значения при содержании кислорода 16 см3 / л, а затем уменьшается. Уменьшение скорости коррозии связано с пассивацией железа кислородом вследствие образования адсорбционной пассивной или Оксидной пленки. [47]
Катодные добавки в неокислительных кислотах повышают скорость коррозии железа. В окислительных кислотах они оказывают слабое влияние. При этом скорость коррозии уменьшается вследствие анодной пассивности металла. [48]
Как показано в разделе 6.1.3, скорость коррозии железа иди стали в природных водах лимитируется диффузией кислорода к поверхности металла. Это утверждение при-ложимо и к коррозии в различных почвах, так как факторы, определяющие скорость почвенной коррозии и коррозии погруженного в воду металла, одинаковы. Таким образом, для этих сред подойдут любые, самые дешевые сталь или железо, лишь бы они обладали требуемой механической прочностью при данной толщине сечения. [49]
Растворенный в воде углекислый газ увеличивает скорость коррозии железа. С этим явлением часто сталкиваются при трактовке механизма котельной коррозии. Основная причина ускоряющего влияния СО2 на коррозию железа в том, что при повышенном содержании в воде СО2 обычно находящиеся в воде ионы кальция не выделяются на поверхности железа в виде плотных и защитных слоев малорастворимых карбонатов ( СаСО3), а остаются в растворе в виде бикарбонатов Са ( НСО3) 2, более растворимых и не оказывающих защитного действия. [50]
Высказанные здесь предположения о причине уменьшения скорости коррозии железа при возрастании частоты переменного тока можно наглядно подтвердить экспериментальными данными, приведенными в таблице. [51]
 |
Влияние рН на скорость коррозии железа в воде. [52] |
При большой концентрации щелочи и повышенной температуре скорость коррозии железа увеличивается. Процесс протекает с образованием анионов гипоферри-та FeO - и выделением водорода. [53]
Известно, что с увеличением концентрации сероводорода скорость коррозии железа или стали возрастает до определенного предела, связанного с ограничением его диффузии к поверхности металла. В условиях жизнедеятельности СВБ таких ограничений не имеется, так как сероводород образуется около поверхности металла и парциальное давление под осадком очень велико. [54]
Бартонь [77] связывает установившуюся ( квазистационарную) скорость коррозии железа во влажной атмосфере ( в присутствии SC 2) с активностью воды в адсорбционной пленке. Активность воды в области относительной влажности воздуха между критической и близкой к 100 % возрастает по закону квадратичной параболы. [55]
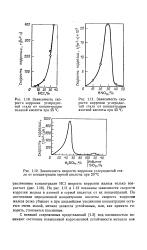
На рис. 1.11 и 1.12 показаны зависимости скорости коррозии железа в азотной и серной кислотах от их концентраций. По достижении определенной концентрации кислоты скорость коррозии железа резко убывает и при дальнейшем увеличении концентрации остается очень малой, металл делается устойчивым, или, как принято говорить, становится пассивным. [57]
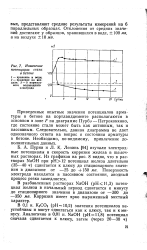 |
Изменение потенциала стали. [58] |
К - Лепинь [94] изучали электродные потенциалы и скорость коррозии железа в щелочных растворах. Из графиков на рис. 8 видно, что в растворах NaOH при рН12 потенциал железа длительно ( 35 - 40 ч) сдвигается к плюсу до стационарного значения в диапазоне от - 25 до 150 мв. Поверхность электрода находится в пассивном состоянии, анодный процесс резко замедляется. [59]
Уменьшение рН раствора при устранении условий пассивности увеличивает скорость коррозии железа и его сплавов, в то время как при рН 13 коррозия железа практически отсутствует. В то же время такие металлы, как молибден, вольфрам, тантал в кислых средах разрушаются меньше, чем в щелочных. [60]
Страницы: 1 2 3 4 5