Скорость - растворение - титан
Cтраница 3
Уменьшения скорости растворения титана при смещении анодного потенциала электрода в положительную сторону при низких частотах, как это наблюдалось в растворах серной кислоты, в данном случае не происходит, так как присутствующие в растворе ионы хлора, очевидно, препятствуют образованию на поверхности металла сплошной пассивирующей окисной пленки. Если при прочих равных условиях сравнить коррозионные эффекты на титане в 10 N растворе H2S04 и в 10 N растворе HG1 при одних и тех же значениях анодного потенциала ( см. рис. 3 и 5), то оказывается, что скорость растворения титана в 10 N НС1 значительно выше ( особенно при низких частотах), чем в серной кислоте той же концентрации. [31]
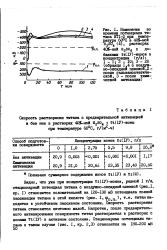 |
Изменение во времени потенциала титана BTI-0 при темпе60 С в 4056-ной. [32] |
Видно, что уже при концентрации т ( 1У) - ионов, равной I г / л, стационарный потенциал титана с воздушно-оксидной пленкой ( рис. 1, кр. I) становится положительней на 120 - 130 мВ потенциала полной пассивации титана в этой кислоте ( рис. I, tpn. Скорость растворения титана становится ничтожно малой. Напротив, после предварительного активирования поверхности титан растворяется в растворах с ионами Т1 ( 1У) в активном состоянии. [33]
Страницы: 1 2 3