Стехиометрия - реакция
Cтраница 2
По стехиометрии реакции мольный поток О2 должен быть в два раза меньше мольного потока СО. Поток азота N2, не участвующего в реакции, должен быть равен нулю. [16]
Если стехиометрия реакции позволяет ожидать достаточно-простую закономерность, часто оказывается целесообразно привлечь для исследования кинетических закономерностей интегральные уравнения скорости реакции, имеющие весьма простой вид для реакции первого, второго и третьего порядков. [17]
Рассмотрение стехиометрии реакций ( 10) - ( 21а) показывает, что ключевые превращения протекают с увеличением объема, а побочные - как с увеличением, так и с уменьшением объема реакционной смеси. Термодинамические расчеты показывают, что изменение общего давления от 0 01 до 1 МПа практически не влияет на состав продуктов. [18]
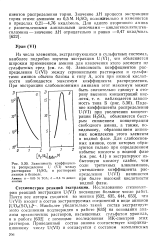 |
Зависимость коэффициен. [19] |
Исследованию стехиометрии реакций экстракции U ( VI) посвящено большое число работ. Наиболее убедительно такой состав экстрагируемого соединения подтвержден в работе [635] на основании анализа органических растворов, насыщенных сульфатом уранила, и в работе [632] с помощью исследования ИК-спектров этих растворов. [20]
Как показывает стехиометрия реакций, на их равновесие можно влиять, изменяя давление. Внутримолекулярной дегидратации, идущей с увеличением числа молей веществ, способствует пониженное или обычное давление. Наоборот, гидратации олефинов благоприятствует высокое давление, увеличивающее равновесную степень конверсии олефина. Зависимость равновесной степени конверсии этилена при его гидратации от давления и температуры изображена на рис. 60, причем аналогичные кривые характерны и для других олефинов. Очевидно, что гидратации способствуют одновременное снижение температуры и повышение давления. [21]
Как показывает стехиометрия реакций, на их равновесие можно илиять, изменяя давление. Внутримолекулярной дегидратации, идущей с увеличением числа молей веществ, способствует пониженное или обычное давление. Наоборот, гидратации олефинов благоприятствует высокое давление, увеличивающее равновесную степень конверсии олефина. Зависимость равновесной степени конверсии этилена при его гидратации от давления и температуры изображена на рис. 62, причем аналогичные кривые характерны и для других олефинов. Очевидно, что гидратации способствуют одновременное снижение температуры и повышение давления. [22]
Отклонение от стехиометрии реакции часто наблюдается при осадительном титровании. Было найдено, что реакция образования PbS при титровании 2 - 150 мкг S2 - раствором РЬ ( ЫОзЬ с 52 - - электродом нестехио метрична вследствие частичной сорбции S2 - на образующемся осадке PbS. Нарушение стехиометрии реакции возможно также за счет образования в процессе титрования низших комплексов. Предложен оригинальный прием, позволяющий повысить точность анализа: титруют F - комллексонатом металла ( М - А1Ш, Сгш, ZrIV, La111 и др.) в присутствии 10 - 100 % - но-го избытка ЭДТА. [23]
Как показывает стехиометрия реакций, равновесие зависит от давления, так как процесс гидратации протекает с уменьшением объема. [24]
После установления стехиометрии реакции химику приходится заниматься изучением зависимостей концентрации каждого из компонентов реакционной смеси от времени. В последующих двух разделах мы рассмотрим случаи, когда аналитическое выражение удовлетворительно описывает поведение рассматриваемых компонентов во времени. Это аналитическое выражение может вытекать либо из точной обработки, либо из серии упрощающих допущений. В обоих случаях сопоставление замеренных во времени концентраций с теоретическими значениями, полученными на основе аналитического выражения, позволяет проверить совпадение исходной гипотезы с экспериментальными данными. [25]
При исследовании стехиометрии реакций применяют растворы титруемого вещества и титранта с известной концентрацией. [26]
 |
Полярограмма восстановления кислорода в насыщенном воздухом 0 1 М растворе КС1. Нижняя кривая - по-лярограмма 0 1 М раствора КС1. [27] |
Как следует из стехиометрии реакций, обе волны имеют равные высоты. [28]
Это известно из стехиометрии реакции. [29]
 |
Данные о скорости реакции иона аммония и нитрит-иона в воде при 25 С. [30] |
Страницы: 1 2 3 4