Стехиометрия - реакция
Cтраница 3
Как следует из стехиометрии реакции (13.5), все эти скорости численно равны друг другу. Определив начальную скорость реакции ( мгновенную скорость в момент времени f 0) для различных исходных концентраций NH и NOJ, можно получить данные, приведенные в табл. 13.2. Эти данные показывают, что изменение [ NH4 ] или [ NO ] приводит к изменению скорости реакции. [31]
ХПК выводятся из стехиометрии реакции денитрификации и из требований к содержанию азота в обработанном стоке. [32]
Прежде всего определим стехиометрию реакций. [33]
Наличие связи между стехиометрией реакции и ее порядком вовсе не является обязательным. Причина заключается в том, что реакции часто протекают в несколько стадий. На каждой из этих стадий кинетика обычно прямо связана с числом соответствующих молекул, но кинетика суммарной реакции не находится в прямой зависимости от числа молекул, подвергающихся конечным превращениям. [34]
Постоянная b дается стехиометрией реакции, а значения DBt / DAi, kAg и kAl могут быть рассчитаны или определены по литературным данным. [35]
 |
Состав сольватов соляной кислоты при экстракции ТБФ по данным, разных авторов. [36] |
Отсутствие надежных сведений о стехиометрии реакций и коэффициентах активности компонентов органической фазы затрудняет Количественное описание экстракции по гидратно-сольватно-му механизму. Поэтому термодинамические константы распределения обычно находят экстраполяцией значений эффективных констант в область бесконечно разбавленных растворов. Их используют в основном для определения коэффициентов активности распределяемого вещества в органической фазе. [37]
Следует заметить, что стехиометрия реакций комплексообразо-вания фенолов с различными электронодонорами зависит от соотношения компонентов. При избытке того или иного компонента наряду с комплексом состава 1: 1 могут образоваться комплексы другого состава. Возможно, что появление некоторых полос в ИК-спектрах этих систем связано с образованием комплексов иного состава. [38]
Конкурирующие реакции кроме нарушения стехиометрии реакции нередко вызывают уменьшение изменения концентрации вблизи точки эквивалентности. Это может обусловить появление труднофиксируемых, ошибочных или несуществующих конечных точек титрования. В случае, когда влияние конкурирующих реакций не столь заметно, его можно ограничить путем более строгого выбора индикаторов. [39]
Наряду со способом определения стехиометрии реакции (1.41), основанным на определении п по уравнению (1.47), состав экстрагируемых соединений обычно исследуется спектрофотометрически. [40]
Особенно плодотворным для выявления стехиометрии реакций и наиболее благоприятных условий их протекания оказались диаграммы, где в зависимости от состава дается выход всех продуктов реакции в отношении каждого из исходных компонентов. Заранее ход реакции было трудно предвидеть, поскольку гидроокись натрия является соединением, достаточно устойчивым и плавящимся без разложения. [41]
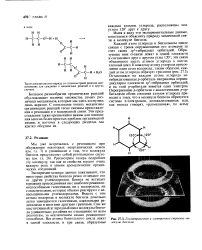 |
Геометрическое и электронное строение молекулы бензола. [42] |
Такое доказательство наряду со стехиометрией реакции дает основание для суждения о механизмах реакций и в других случаях. [43]
В связи с этим учет стехиометрии реакций является необходимым условием правильного термодинамического анализа предпочтительности реакций в одной и той же системе, что дает возможность при использовании надежных исходных термохимических данных получить абсолютные энергетические характеристики образования конечных, наиболее вероятных и устойчивых соединений. Для обеспечения этих условий нами предложен и проверен на целом ряде реакций в различных системах принцип расчета по составам. [44]
Первое из них есть отражение стехиометрии реакций ( 1), ( 2), совпадающее в данном случае с уравнением электронейтральности, а второе заменяет уравнение ( 3) в нужных нам терминах. Необходимо записать четыре уравнения связи в тех же терминах. [45]
Страницы: 1 2 3 4