Триол
Cтраница 3
Естественным распространением метода образования ацетони-дов является получение ортоэфиров из триолов соответствующего строения. [31]
При под-кислении этих щелочных растворов получается соединение СюНнОз, представляющее собой триол, и два других продукта, CioHieOs и CioHieOe, строение которых не выяснено. Термическое разложение продуктов аутоокисления при 100 С дает гликоль ( XXIX) и вещество, имеющее формулу CooHjcOe. Было найдено, что эпоксидное соединение ( XXX), соответствующее этому гликолю, его изомер ( XXXI) и кетон, полученный в результате перегруппировки, находятся в низкокипящих фракциях оксидата. [32]
Изменение количества сшивающего агента от 0 33 до 0 22 моль триола на 1 моль преполимера приводит, как и можно было ожидать, к снижению напряжения при удлинении 100 % и сопротивления разрыву и к увеличению относительного удлинения. Уменьшение плотности химической сетки в вулканизатах способствует большему проявлению эффекта полидисперсности диеновой составляющей. [33]
Триол-I, который образует лишь моноацетильное производное аоа, легко перегруппировывается803 в триол - Н, дающий диацетильное производное. [34]
При гидролизе трн-хотеколона ( 438) кипящей 0 1 N НС1 получается триол ( 445), который, судя по его отношению к ШО4, не содержит а-гликольной группировки. [35]
Наилучшие результаты получены при использовании в качестве сшивающих агентов ароматических диолов или триолов. [36]
При по; кислении этих щелочных растворов получается соединеш CioHH03, представляющее собой триол, и два других продукт CioHieOs и CioHieOe, строение которых не выяснено. [37]
Если нужно получить сшитый полимер, лучше применять трнефункциональный реагент ( например, триол) и катализатор, ускоряющий только реакцию изоцианата с гидроксилом. Преимущество этого метода состоит в том, что поперечные связи такого полимера более термоста-бильиы, чем биуретовые или аллофанатные. [38]
Если нужно получить сшитый полимер, лучше применять трифункциональный реагент ( например, триол) и катализатор, ускоряющий только реакцию изоцианата с гидроксилом. Преимущество этого метода состоит в том, что поперечные связи такого полимера более термостабильны, чем биуретовые или аллофанатные. [39]
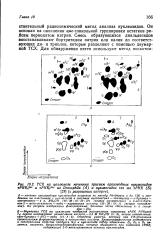 |
ТСХ на целлюлозе меченных тритием производных нуклеозидов. [40] |
Смесь образующихся диальдегидов восстанавливают бортритидом натрия или калия до соответствующих ди - и триолов, которые разделяют с помощью двумерной ТСХ. [41]
Для получения полиэфирных пленкообразователей с неомыляемой цепью применяют переэтерификацию те-ломеров стиролакриловой кислоты с триолом и ненасыщенными гидроксилсодержащими соединениями [43], взаимодействие карбоксилсодержащих теломеров малеи-нового ангидрида и октена или малеинового ангидрида и стирола с последующей соконденсацией с меламиноформ-альдегидной смолой [44] и другие способы. [42]
Реакции переэтерификации триэфиров и триамидов фосфористой кислоты применяют для получения жестких каркасных триэфиров из триолов. Оба соединения используют в синтезе моноциклических эфиров тетра-координированного фосфора заданной конфигурации. [43]
Химизм этой реакции неизвестен, но, вероятно, она основана на образовании сольвата триола с трихлоруксусной кислотой. Эфиры 7-дегидростеринов реагируют так же, как соответствующие стерины. [44]
В какой-то незначительной степени происходит, по-видимому, отщепление и третьей молекулы воды от дегидратируемого триола, но образующийся триениновый углеводород в условиях реакции полимеризуется в смолообразный продукт и в свободном состоянии выделен не был. [45]
Страницы: 1 2 3 4