Формула - лондон
Cтраница 3
Каковы основные предположения, используемые в полуэмпирическом методе расчета поверхности потенциальной энергии, основанном на формуле Лондона и ее обобщениях. [31]
И тот и другие использовали выражение для молекулярного взаимодействия, получающееся путем интегрирования парных взаимодействий, описываемых формулой Лондона, по объемам обеих частиц. [32]
В случае, когда толщина прослойки становится больше X - длины волны, соответствующей переходу между основным и возбужденным состоянием атома, формулы Лондона, как следует из теории Казимира-Польдера [3], становятся неприложимыми в связи с конечной скоростью распространения электромагнитных сил. В результате на больших расстояниях дисперсионные силы убывают на одну степень расстояния быстрее. [33]
Если R велико ( R hc / A, где Л - характерная энергия возбуждения молекулы), зависимость R - - 6 заменяется на R-7 и сила взаимодействия уменьшается значительно быстрее, чем предсказывает формула Лондона. [34]
Формула Лондона (2.44) для всех инертных атомов дает заниженные значения С &: Формула Слейте-ра - Кирквуда (2.46) для легких атомов дает оценку сверху, для тяжелых - оценку снизу, но ближе к точному значению, чем формула Лондона. [35]
 |
Сравнение значений С0 и С8 для системы АгН, полученных методом МК ССП и другими методами ( в ат. ед. [36] |
Поляризуемость связи является анизотропной величиной; в выражение для дисперсионной энергии входит поперечная поляризуемость а-1 - и разность продольной и поперечной поляризуемостей 6 all - a - 1, в качестве последних рекомендуется брать экспериментальные значения. Для входящих в формулу Лондона энергий возбуждения рекомендуется брать удвоенные значения потенциалов ионизации. [37]
Для Н Br-взаимодействий Достровский, Хюджес и Ингольд [30] выбрали р 0 345 путем сравнения с величиной, полученной Борном и Майером [18] из исследований кристаллической структуры ряда галогенидов щелочных металлов. Константа А была рассчитана по формуле Лондона, а значение В определено из условия минимума 8 при г 3 55 А. [38]
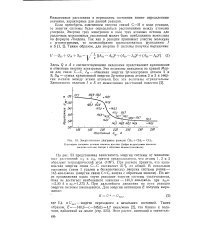 |
Энергетическая диаграмма реакции СН3 СН2 СН2. [39] |
Энергия трех электронов в поле трех атомных остовов для различных межатомных расстояний может быть приближенно вычислена по формуле Лондона. [40]
Величина I, ограничивающая снизу диапазон классической зависимости сечения от угла рассеяния, оказывается достаточно большой. Оценим эту величину, например, для ван-дер-ваальсов-ского взаимодействия при комнатной температуре. Константу взаимодействия можно оценить по формуле Лондона (2.102) величиной a06RyBiB2 ( 1 2 - поляризуемости атомов в атомных, единицах); эти величины сильно зависят от сорта и состояний атомов и изменяются в пределах от единиц до сотен. [41]
Значения с, полученные с помощью вириальных коэффициентов и различных теоретических соображений, лежат в широких пределах. В случае атомов и молекул, для которых известны более точные экспериментальные значения с, величины с, найденные с помощью формулы Кирквуда - Мюллера, имеют даже несколько большее значение. Значение коэффициента с, получаемое с помощью формулы Лондона, часто оказывается меньше в два раза. Коэффициент с Слэйтера - Кирквуда лучше лондоновского, но также недооценивает эту величину. [42]
Не надо забывать, однако, что принятая для г0 величина 3 7А может быть слишком высока, делая вычисленные величины у слишком малыми, и что пренебрежение квадруполь-ди-полъным членом также делает у слишком низким. Возможно, что более точное вычисление дало бы лучшее согласие с формулой Лондона. Во всяком случае рассмотренные вычисления являются еще слишком неточными, чтобы можно было определенно решить, какой из трех методов дает лучшее соответствие с опытом. [43]
Баррер пришел к заключению, что лучшее согласие с опытом дает формула Кирквуда. Не надо забывать, однако, что принятая для г0 величина 3 7А может быть слишком высока, делая вычисленные величины ср слишком малыми, и что пренебрежение квадруполь-ди-польным членом также делает р слишком низким. Возможно, что более точное вычисление дало бы лучшее согласие с формулой Лондона. Во всяком случае рассмотренные вычисления являются еще слишком неточными, чтобы можно было определенно решить, какой из трех методов дает лучшее соответствие с опытом. [44]
Рассмотрим снова в качестве примера пиридин. Но для таких значений R, по порядку сравнимых с размерами невозбужденных молекул, формула Лондона заведомо неприменима. [45]
Страницы: 1 2 3 4