Энергия - активация - распад
Cтраница 2
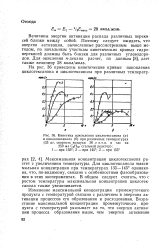 |
Кинетика накопления циклогексанона ( и и циклогексанола ( б при различных температурах ( 33 ат, скорость воздуха 38 л н.т.д. в час на. [16] |
Величины энергии активации распада различных перекисей близки между собой. Поэтому следует ожидать, что-энергии активации, вычисленные рассмотренным выше методом, по начальным участкам кинетических кривых гидроперекисей должны быть близки для различных углеводородов. Для окисления н-декана расчет, по данным [8], дает также величину 28 ккал / моль. [17]
Значения энергии активации распада активных центров первого и второго типа равны 30 6 и 16 75 кДж / моль соответственно. Оказалось, однако, что значения прещэкопоненциальных множителей в обоих случаях сильно отличаются от значения предэкопонен-циального множителя мономолекулярадой реакции. [18]
Большая величина энергии активации распада углеводородов также приводит к заключению, что реакции термич. [19]
Соответственно зависимость энергии активации распада триоксида от полярности среды выражена в большей степени. [20]
При отсутствии аминов энергия активации распада гидроперекиси полипропилена равна 25 ккал / моль, в присутствии дифениламина - 17 ккал / моль, N - циклогексил - N1 - фенил-п-фенилендиамина - 14 ккал / моль. [21]
 |
Зависимость времени до разрушения по - 10 tttft. С листирола от обратной температуры [ 721 f. [22] |
В этих местах энергия активации распада межатомных связей понижается особенно сильно. Именно в этих местах наиболее интенсивно идут процессы термофлюктуационного разрыва напряженных связей. [23]
Предэкспоненциальный множитель и энергия активации распада полустабильных промежуточных веществ [ уравнение ( 56) ] сопоставимы со значениями, которые обычно принимаются для гидроперекисей. [24]
Предэкспоненциальный множитель и энергия активации распада полустабильных промежуточных веществ [ уравнение ( 56) 1 сопоставимы со значениями, которые обычно принимаются для гидроперекисей. [25]
Под действием растягивающих усилий энергия активации распада связей должна уменьшиться. Говоря о распаде напряженных макромолекул, прежде всего, конечно, следует иметь в виду перенапряженные связи. [26]
Энергия диссоциации связи равна энергии активации распада молекулы на радикалы, так как обратная реакция соединения радикалов идет с нулевой энергией активации. [27]
Как уже отмечалось, энергия активации распада гексафенил-этана на радикалы составляет 18 - 19 ккал / моль, энергия связи - около 11 ккал / моль. Это означает, что рекомбинация радикалов связана с преодолением активационного барьера. [28]
Это означает, что энергия активации распада переписного радикала больше энергии активации его взаимодействия с исходным углеводородом с образованием алкилгидро-перекиси. [29]
Заметим, что снижение энергии активации распада вторичн. С - Н в бромиде уменьшает энергию активации молекулярного распада ( см. стр. [30]
Страницы: 1 2 3 4