Энергия - активация - распад
Cтраница 3
 |
Схема распада срединного макрораднкала. [31] |
Стрелка указывает на связь со сниженной энергией активации распада; б) пояснение структуры и обозначений для двойной ( СС) связи. [32]
Рассматривая работы, в которых определялась энергия активации распада ацетила, необходимо указать еще на исследование Шварца [89], изучившего пиролиз ацетона в присутствии толуола. [33]
По величинам потенциалов появления ими вычислены энергии активации распада первичных ионов различными путями. Рассмотрены также вероятные внутримолекулярные перегруппировки с переходом водорода, допущение которых необходимо для объяснения появления, различных осколочных ионов. [34]
По величинам потенциалов появления ими вычислены энергии активации распада первичных ионов различными путями. Рассмотрены также вероятные внутримолекулярные перегруппировки с переходом водорода, допущение которых необходимо для объяснения появления различных осколочных ионов. [35]
Теория Портера позволяет ожидать относительно низких значений энергии активации распада даже в отсутствие каталитических эффектов. Другими словами, согласно [65], прямой элементарный распад углеводородов ( даже таких простых, как бензол и этилен) при высоких температурах маловероятен. [36]
Однако родственность энергии активации разрушения полимеров с энергией активации распада химических связей подтверждается и качественно рядом опытов, описанных в гл. [37]
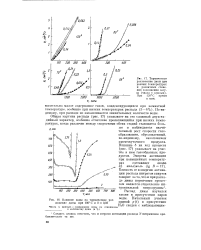 |
Влияние воды на термическое разложение дины при 100 С и б 0 03. [38] |
Следует, однако, отметить, что и энергия активации распада N-нитраминов приблизительно та же. [39]
С и по их зависимости от температуры определена энергия активации распада хлорной кислоты на первой стадии: Е 32 6 ккал / моль. [40]
Точно таким же способом можно оценить нижнюю границу для энергии активации распада по С - Н - связи. [41]
Энергия активации термораспада неконцевых хлораллиль-ных структур ПВХ [420] меньше энергии активации распада низкомолекулярных модельных соединений [642] на 5 - 6 ккал / моль, что может быть связано с влиянием среды, так как фрагменты макромолекул распадаются в полярной полимерной фазе, что снижает энтальпию образования переходного комплекса. [42]
Мною было показано на основе анализа экспериментальных данных, что энергия активации распада С2Н5Вг составляет 49 - 50 ккал. [43]
Мною было показано на основе анализа экспериментальных данных, что энергия активации распада С2Н6Вг составляет 49 - 50 ккал. [44]
Из приведенных данных, а также из того факта, что энергия активации распада на АСК большая ( около 20 - 30 ккал / моль), следует целесообразность раздельного каталитического крекинга парафинистого прямогонного и ароматизированного сырья в отдельных ступенях. [45]
Страницы: 1 2 3 4