Энергия - гиббс
Cтраница 2
Энергия Гиббса служит критерием самопроизвольного протекания химической реакции при изобарно-изотермических процессах. [16]
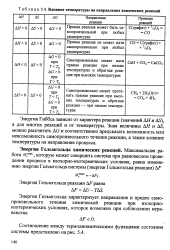 |
Влияние температуры на направление химических реакций. [17] |
Энергия Гиббса зависит от характера реакции ( значений А / f и AS), а для многих реакций и от температуры. [18]
Энергия Гиббса является функцией состояния системы, и ее изменение не зависит от пути проведения процесса, а зависит только от начального и конечного состояния системы. Она является однозначной, непрерывной и конечной функцией от параметров состояния. [19]
Энергия Гиббса с повышением давления при Tconst растет. [20]
Энергия Гиббса является экстенсивной функцией. [21]
Энергии Гиббса для приведенных реакций означают, что РС1з и AsCl3 подвергаются гидролизу и первая реакция более необратима, чем вторая. [22]
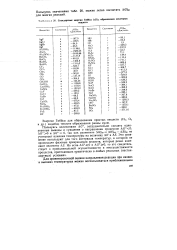 |
Стандартные энергии Гиббса ДОив образования некоторых. [23] |
Энергии Гиббса для образования простых веществ ( На, СЬ и др.) подобнр теплоте образования равны нулю. [24]
Энергии Гиббса для приведенных реакций означают, что РСЬ и AsCU подвергаются гидролизу и первая реакция более необратима, чем вторая. [25]
Энергия Гиббса некоторой системы выражается уравнением G аТ ( - In7) ВТ пР - СТ. [26]
Энергия Гиббса задается уравнением (6.19); для систем, стремящихся к состоянию равновесия ( обратимый процесс), она убывает ( AG0) и при достижении равновесия ( АС 0) энергия Гиббса принимает минимальное значение. [27]
Энергия Гиббса ( изобарный потенциал) такой системы при любом необратимом процессе убывает, а при обратимом процессе сохраняет постоянное значение. [28]
Энергия Гиббса задается уравнением (6.19); для систем, стремящихся к состоянию равновесия ( обратимый процесс), она убывает ( ДС0) и при достижении равновесия AG0, а сама энергия Гиббса принимает минимальное значение. [30]
Страницы: 1 2 3 4