Энтальпий
Cтраница 2
Этими выражениями для энтальпий обычно пользуются при расчетах. [16]
Приведем табл. 25 энтальпий образования некоторых часто встречающихся газовых компонент при ОК. [17]
Зная разность, энтальпий сгорания, легко определить разность энтальпий образования органического вещества. [18]
В качестве же энтальпий образования азидов стронция и кальция в литературе [8] принимаются взятые с обратным знаком изменения энтальпий, сопровождающие протекающие со взрывом процессы тер-ъшческого разложения SrNe и CaNe. [19]
Изображение теплоты процесса и энтальпий в виде площадей весьма наглядно, что и является преимуществом Т - диаграммы перед диафаммами другого вида. Однако для получения количественных результатов необходимо производить измерения и вычисления площадей, что практически усложняет расчет и снижает его точность. [20]
Проблема оценки энтропии и энтальпий методами, основанными на использовании температур плавления, состоит в том, что в настоящее время мы не располагаем методами расчета этих параметров как функции относительного содержания неметалла и металла. Данные табл. 31 показывают, что энтропия NbCi уменьшается почти на 15 % при изменении состава от NbCi0 до NbCo7 - В пределах этой области составов существует только одна точка, в которой наблюдается конгруэнтное плавление, и поэтому нельзя определить температуру плавления для препаратов иных составов. Это обстоятельство и эмпиризм такого подхода особенно подчеркивают необходимость экспериментальных определений величин ( SMS. [21]
Для подсчета энергий ( энтальпий) изомеризации нет необходимости находить энтальпии атомизации, суммируя энтальпии связей, - достаточно лишь сравнить энергии напряжения, которые были получены минимизацией потенциальных функций молекул. [22]
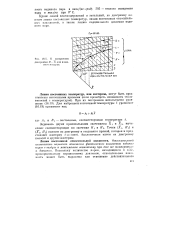 |
К построению диаграммы Н-X для влажного воздуха. [23] |
Кроме линий влагосодержаний и энтальпий, на диаграмму наносят линии постоянных температур, линии постоянных относительных вла / кностей, а также линию парциального давления водяного пара. [24]
Кроме линий влагосодержаний и энтальпий, на диаграмму наносят линии постоянных температур, линии постоянных относительных влажностей, а также линию парциального давления водяного пара. [25]
Помимо стандартных энтропии и энтальпий состояния, термохимическое описание свойств материала требует информации о теплоте образования при 298 15 К и изменении энтальпии в интервале от 298 15 К до какой-то интересующей нас температуры. Теплоты образования можно определить калориметрически; карбид или нитрид превращается сжиганием в окисел, и выделяющееся при этом тепло измеряется. Изменение энтальпии обычно определяется с помощью калориметра смешения. Эти характеристики карбидов и нитридов существенно меняются с отклонением состава соединения от стехиометрического, что трудно оценить с достаточно высокой степенью точности. Экспериментальное исследование зависимостей от состава представляет очень сложную задачу, поскольку связано с работой при очень высоких температурах и трудностью контроля составов. Большинство измерений было выполнено на образцах, составы которых близки к стехиометри-ческим. [26]
Характер изменения констант и энтальпий диссоциации при вариации противоиона и растворителя соответствует обычным представлениям. Например, поскольку величина din D / d n T для тетрагидропирана равна - 0 97, теплота диссоциации, согласно выражению ( 3), должна быть близка к нулю, что и наблюдается. [27]
А - перепад - энтальпий углекислоты в конденсатор-испа-рителе, ккал / кг. [28]
Знание теплот реакции ( энтальпий реакции А / /) представляет интерес по двум причинам: для оценки содержания энергии в молекулах и для предсказания хода химических реакций. В настоящем разделе мы рассмотрим первый из этих аспектов. [29]
Знание теплот реакции ( энтальпий реакции ДЯ) представляет интерес по двум причинам: для оценки содержания энергии в молекулах и для предсказания хода химических реакций. В настоящем разделе мы рассмотрим первый из этих аспектов. [30]
Страницы: 1 2 3 4