Энтальпий
Cтраница 4
Использование значений среднелогарифмических напоров температур и энтальпий осложняет проведение расчетов. [46]
ДЯ представляет собой разность теплосодержаний ( энтальпий) конечных продуктов реакций и исходных веществ. Теплосодержание - это свойство вещества, оно является мерой энергии, накапливаемой веществом при его образовании. В этом заключается физический смысл величины ДЯ. Долгое время тепловые эффекты обозначали через Q и считали их положительными, если выделяется теплота, и отрицательными, если она поглощается. Следует придерживаться первого обозначения тепловых эффектов через ДЯ, поскольку оно введено для единообразия с другими дисциплинами. [47]
В расчетах тепловых эффектов ( или энтальпий) химических реакций можно мысленно представить себе такой ход реакций: сначала исходные вещества разлагаются на элементы, и все энтальпии суммируются с соответствующими знаками; затем элементы соединяются с образованием конечных веществ, и энтальпии снова суммируются; разность сумм энтальпий и дает нам энтальпию реакции согласно следствию из закона Гесса. [48]
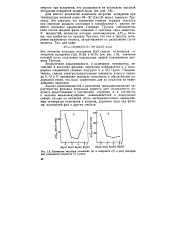 |
Изменение энтропии плавления ( а и испарения ( б в ряду водород - ных соединений элементов VI группы. [49] |
Аналогичная закономерность в изменении температур, энтальпий и энтропии фазовых переходов наблюдается и у водородных соединений главных подгрупп V и VII групп. Следовательно, сильно электроотрицательные элементы второго периода F, О и N проявляют высокую склонность к образованию водородной связи, что мало характерно для их аналогов из нижележащих периодов. [50]
ДЯ представляет собой разность теплосодержаний ( энтальпий) Я конечных продуктов реакции и исходных веществ. [51]
Ниже рассмотрена методика расчета температур и энтальпий по газовому тракту от выхода из топочной камеры до сечения газохода за водяным экономайзером применительно к парогенераторам сверхкритического давления. Эта методика может быть использована и для парогенераторов докритического давления, за исключением элементов, состоящих из развитых кипятильных поверхностей нагрева. [52]
Будут ли закономерности, найденные для энтальпий атомизации, справедливы для энергий. Поскольку изменения всех неизвестных величин, входящих в уравнение (4.2), невелики для молекул, состоящих из одного и того же количества атомов углерода и водорода ( разумеется, это касается не только углеводоро-цов), то на поставленный вопрос можно дать положительный ответ. Но при этом следует ожидать погрешностей порядка 0 2 - 1 0 ккал / моль, связанных прежде всего с пренебрежением нуле-зыми колебаниями. [53]
Знание этих продуктов и соответствующих им энтальпий реакций при использовании закона Гесса позволяет вычислить энергетические характеристики связей и межмолекулярных взаимодействий. [54]
Рециркуляция газов в расчетах объемов и энтальпий продуктов сгорания учитывается на тракте от места ввода рециркулирующих газов в котельный агрегат до места их отбора. [55]
Определение объемов воздуха, состава и энтальпий продуктов сгорания производится по рекомендациям [45] или по упрощенной методике теплотехнических расчетов. [56]
Страницы: 1 2 3 4