Стерический эффект
Cтраница 3
Среди различных стерических эффектов, приводящих к снижению интенсивности поглощения, при работе с природными соединениями наиболее часто приходится сталкиваться со снижением интенсивности поглощения сопряженных систем, вызванным наличием объемистых заместителей, в частности метильных групп ( ср. [31]
Помимо стерических эффектов заместителей, скорость конденсации зависит от их полярного влияния и от природы катализатора. [32]
Вследствие большого стерического эффекта группы [ Сг ( СО) з ] реакция в образовавшемся jt - комплексе протекает только с экзо-стороны ароматического цикла ( не участвующей в комплексообразовании) или боковой цепи, что обеспечивает высокую стереоселективность в реакциях с использованием комплексов этого типа. [33]
По-видимому, стерический эффект играет важную роль в реакциях органических комплексов пентамминкобальта ( Ш) и не всегда удается получить наилучшую геометрию для максимального сопряжения. В случае полуэфирных терефталатных комплексов введение заместителей в 2 6-положение понижает константу скорости восстановления, протекающего путем атаки на соседний атом. [34]
Необходимость учета стерических эффектов при объяснении поглощения сопряженными системами в ультрафиолетовой области очень хорошо иллюстрируется на примере метилионона. [35]
Специфика проявления стерических эффектов в гетероаромати-ческом ряду часто связана с наличием гетероатома. Так, пиридин, 2 6-диметилпиридин и 2 6-диизопропюширидин при действии триоксида серы в жидком SO2 при - 10 С образуют продукты присоединения молекулы SO3 по атому азота - пириди-ний-сульфотриоксиды. В них заряженный гетероатом пассивирует кольцо по отношению к дальнейшему сульфированию. Очевидно, что две объемистых трег-бутильных группы препятствуют координации пиридинового азота с молекулой SO3, в силу чего сульфироваться может нейтральное основание. [36]
При отсутствии стерических эффектов и эффектов сопряжения катионы класса ( а) обладают способностью к координации в последовательности NPAsSb; OS; FClBrI, а для ряда однотипных лигандов NRa, RzO и RF - в последовательности N О F. Вследствие образования обратной двойной связи, а также увеличивающейся поляризуемости и уменьшения отталкивания неподеленной пары электронов заполненными я-орби-талями металла различия в ряду Р S С1 менее глубоки. [37]
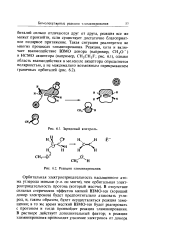 |
Зарядовый контроль.| Реакция элиминирования. [38] |
В отсутствие сильных стерических эффектов мягкий ВЗМО-ген ( хороший донор электронов) будет предпочтительно атаковать углерод, и, таким образом, будет осуществляться реакция замещения; в то же время жесткий ВЗМО-ген будет реагировать с протоном и тогда произойдет реакция элиминирования. [39]
Несмотря на близость стерических эффектов в сериях ( 8 - 6) и ( 8 - 7), при переходе от катализируемого кислотами сольволиза к сольволизу, катализируемому основаниями, р становится заметно более положительным. В рассматриваемых сериях влияние на р или р замены катализатора становится более очевидным при сравнении с соответствующими изменениями, которые вызывает замена кислотного катализатора на основной при гидролизе органических сложных эфиров. Для последнего р становится более положительным - на 2 48 единицы. Для серий ( 8 - 1) и ( 8 - 5) изменение р составляет 3 53 единицы, для серий ( 8 - 6) и ( 8 - 7) - 3 9 единицы. [40]
Если отвлечься от стерических эффектов, то вся совокупность опытных данных указывает на существование двух факторов, определяющих скорость радикальных реакций. [41]
Однако важность этих стерических эффектов обычно не легко оценить. [42]
Если отвлечься от стерических эффектов, то вся совокупность опытных данных позволяет выделить два фактора, определяющих зависимость скоростирадикальныхреакций от строенияреагирующихмолекул и радикалов. RH) и радикалов и антибатность этих рядов. Эта концепция применима, в первую очередь, к углеводородам, но с некоторыми оговорками и ограничениями оно может быть распространено и на молекулы, содержащие гетероатомы. [43]
Для количественной характеристики стерического эффекта заместителей воспользовались реакционной серией кислотнокатали-тического гидролиза сложных эфиров, которая почти не чувствительна к индуктивному эффекту заместителей. [44]
Глубокий анализ этих стерических эффектов строения щелочных стекол, простых и смешанных видов, дан Дитцелем и Шейбани ( A. Особенно важное значение имеют максимумы плотности смешанных силикатных стекол вблизи отношения обеих щелочей 1: 1, что служит указанием на взаимную поляризацию ионов. [45]
Страницы: 1 2 3 4