Выход - перекись - водород
Cтраница 3
При облучении такой системы - лучами наблюдается увеличение выхода перекиси водорода в 3 - 5 раз по сравнению с выходом в том же растворе, но без сенсибилизатора. [31]
При повышении температуры раствора, продолжительном сни жении выхода перекиси водорода и прекращении подачи воздух; в окислители необходимо отключить подачу пара в секционны рубашки, проверить исправность регулирующего клапана на лиши азота и включить подачу охлаждающей воды в трубчатые тепло обменники окислителя. Если этих мер недостаточно, нужно: подат ] дистиллированную воду в I и II секции окислителя и прекратит ] подачу изопропилового спирта, одновременно необходимо слить ре акционную смесь из окислителя в аварийную емкость. [32]
Если в растворе присутствует вещество, способное окисляться, выход перекиси водорода уменьшается. Если растворенное вещество является окислителем, то его присутствие уменьшает выход молекулярного водорода. Это легко понять, если считать, что Н2 и Н202 образуются, по крайней мере частично, в результате рекомбинации одинаковых радикалов, возникающих близко друг от друга. Молекулы растворенного вещества, присутствующие в растворе и способные вступить во взаимодействие с Н или ОН, стремятся помешать этой рекомбинации. [33]
Выявлено, что ацетон на скорость процесса п на выход перекиси водорода не влияет. Уксусная же кислота, не влияя на выход перекиси водорода, оказывает тормозящее действие на окисление изопропилового спирта. [34]
Повышение давления до 2 ата практически не сказывается на энергетических и материальных выходах перекиси водорода. Увеличение давления до 3 ата вызывает падение выходов и концентрации перекиси водорода. [35]
Удаляя эти продукты из зоны реакции, можно значительно повысить выход перекиси водорода при окислении циклогекса-нола. [36]
При взрывном окислении водорода [6] нами было установлено, что на выход перекиси водорода влияют соотношение Н2: 02 и диаметр реакционного сосуда, как это наблюдается и в случае диффузионного пламени. [37]
Изучено большое число диэлектрических материалов с точки зрения влияния их на выход перекиси водорода по энергии; наиболее удовлетворительными оказались кварцевые пластины. [38]
При изменении давления в реакторе изменяются высота и положение максимума кривых выхода перекиси водорода на пропущенный кислород а. Наибольшее значение а ( 42 %) получено при 2 ата. [39]
Так как СНго, 0 725, GH 0 5, то выход перекиси водорода численно равен G ( Н202) - 0 97 молекул / 100 эв. [40]
При изучении влияния температуры показано, что в пределах - 35 8 выход перекиси водорода ( по кислороду) и ее концентрация практически не изменяются. При 8 получена 80 % - пая перекись водорода. Вычислена энергия активации реакции образования перекиси водорода в тихом разряде, равная 1200 кал / моль. Такое низкое значение совпадает с энергией активации при фотохимическом образовании перекиси, что указывает на общие черты активации в обоих случаях. [41]
При изучении влияния температуры показано, что в пределах от - 35 до 8 выход перекиси водорода ( по кислороду) и ее концентрация практически не изменяются. Вычислена энергия активации реакции образования перекиси водорода в барьерном разряде, оказавшаяся равной 1200 кал / моль. [42]
При изучении влияния температуры показано, что в пределах - 35ч - 8 С выход перекиси водорода ( по кислороду) и ее концентрация практически не изменяются. При 8 С получена 80 % - ная перекись водорода. Вычислена энергия активации реакции образования перекиси водорода в тихом разряде, равная 1200 кал / моль. Такое низкое значение совпадает с энергией активации при фотохимическом образовании перекиси, что указывает на общие черты активации в обоих случаях. Обнаружено увеличение потребления кислорода на образование Н2О2 при уменьшении содержания кислорода, а также благоприятное влияние добавок водяного пара ( 100 мм рт. ст.) и резко отрицательное влияние добавок азота. Аргон в малых концентрациях как будто бы. [43]
При горении метана в кислороде выход озона увеличивается с увеличением количества избыточного кислорода, хотя выход перекиси водорода и формальдегида тцэи этом уменьшается. Если кислород горит в метане, то выход перекиси водорода и здесь уменьшается, но выход формальдегида растет с увеличением количества избыточного метана. При этом совершенно не образуется озона. Механизм образования этих продуктов предполагает разложение метана на метилен ( СН2) и атомный водород. Атомный водород образует главным образом молекулярный водород и некоторое количество перекиси водорода. Метилен частью сгорает в окись углерода и формальдегид. Дальнейшее окисление этих продуктов дает воду и двуокись углерода. [44]
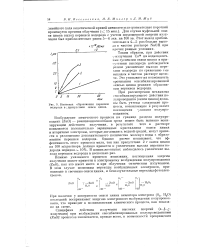 |
Кинетика образования перекиси водорода в [ присутствии окиси цинка. [45] |
Страницы: 1 2 3 4