Габер
Cтраница 3
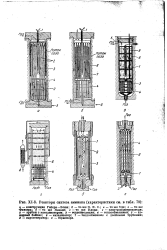 |
Реакторы синтеза аммиака ( характеристики в 79. [31] |
Габера - Боша; б - то же N. Уде; г - то же Фаувера; в - то же Казале; е - то же Клода; 1 - электроподогреватели; Я - трубки с катализатором; 3 - теплоизоляция; 4 - теплообменники; s - хо-додный байпас; в - катализатор; 7 - теплообменник с двойными трубками; в - парогенератор; - термопара. [32]
Габера) для этого вещества значительно уже. [33]
Габера, так как АЯ0бР, ДЯат, ДЯДИсс и / обычно бывают известны. [34]
Габера, а именно, на вопросе об устойчивости различных валентных форм соединений металлов. В энергетику ионного кристалла вносит свой вклад целый ряд факторов, а не только энергия атомизации металла, как у соединений ковалентного типа. Попробуем на основании цикла Борна - Габера понять, почему низковалентные формы металлов мало устойчивы. [35]
Габера, Клода и других. Вполне понятно, что синтез под низкими давлениями при достаточном выходе аммиака представил-бы огромные преимущества, упростив все процессы и всю аппаратуру, и, по его осуществлении в технике, нынешние методы его получения ока - Зались-бы устаревшими или даже ненужными. [36]
Габера процесс - реакция синтеза аммиака из водорода и азота, оптимальные условия проведения которой ( температура, давление, катализатор) разработаны Фрицем Габером. [37]
Габеру в опытах по разложению масляного - газа удалось приготовить из гексана нафтены. [38]
Габером [5] измерена электродвижущая сила водородно-кислородной цепи при температурах 300 - 1000 С, с использованием в качестве электролитов расплавленных щелочей, стекла и фарфора, и показана обратимость этих цепей при высоких температурах. [39]
Габером и с 1913 г. является практически единственным способом фиксации азота. [40]
Габером и его сотрудниками было испробовано большое число катализаторов: церий и сплавы или специальным образом приготовленные смеси его с железом, марганцем, лантаном; марганец, приготовленный из амальгамы марганца; осмий, рутений, уран, вольфрам, молибден и другие металлы. Вот, несколько дан ных, касающихся применения катализаторов, величины давления и полученных концентраций аммиака при различных, постоянно поддерживаемых температурах реагирующих веществ. [41]
Фриц Габер ( 1868 - 1934), профессор и директор Института физической химии в Мюнхена ( Бавария), профессор физики и электрохимии в Берлине. [42]
Фриц Габер ( 1868 - 1934), профессор и директор Института физической химии в Мюнхене ( Бавария), профессор физики и электрохимии в Берлине. [43]
Впоследствии Габер отказался от своей схемы и признал, что как в присутствии, так и в отсутствии воды окисляемое вещество присоединяет целую молекулу кислорода. [44]
Впоследствии Габер и Вейс [4] сообщили, что даже при столь малых концентрациях реагента, как 10 - 3 моля, в нейтральных растворах для п получаются значения, равные 15 и большие. Такие высокие расходные коэффициенты, не наблюдавшиеся предыдущими исследователями, были приписаны применению более эффективного способа перемешивания. [45]
Страницы: 1 2 3 4