Резонансный гибрид
Cтраница 2
Реальную молекулу бензола обычно рассматривают как резонансный гибрид, в котором распределение электронной плотности является промежуточным между распределением электронной плотности в резонансных структурах. Как пример изображения резонансного гибрида выше показаны две формулы бензола: Полинга и Робинсона. [16]
В частности, структура VIII является резонансным гибридом, в котором поровну участвуют структуры III и VII. [17]
Парарозаншган и другие трифенилметановые красители являются резонансными гибридами; в большинстве входящих в них структур положительный заряд несет один из атомов азота или центральный атом углерода. [18]
Диполярные структуры принимают значительное участие в резонансных гибридах этих веществ. Распределение зарядов таково, что углеродные атомы в циклах с одним гетероатомом получают частичный отрицательный заряд. [19]
Диполярные структуры принимают значительное участие в резонансных гибридах этих веществ. Распределение зарядов таково, что углеродные атомы в циклах с одним гетероатомом получают частичный отрицателт. [20]
Такая структура в методе ВС представляется как резонансный гибрид ( см. 12.IV, стр. МО предполагается, что азот образует три сг-связи, используя 5р 2-гибридные орбитали, а комбинация р2 - орбиталей атома азота и трех атомов кислорода дает связывающую л - МО, занятую двумя электронами. [21]
 |
Изображение распределения зарядов я-электронов в электронной оболочке бензола ( 12 - 1, стр. 163. [22] |
В настоящее время принято представлять бензол как резонансный гибрид, состоящий из двух структур Кекуле. [23]
Вклад форм типа ( в) в резонансный гибрид в этом случае намного меньше, чем в случае обычных сложных эфиров, вследствие чего электрофильность углеродного атома карбонильной группы существенно повышается. Типичными нуклеофилами в биологических системах являются амины, карбоксильные ионы, фосфат-ионы и карбанионы, которые обсуждаются ниже. [24]
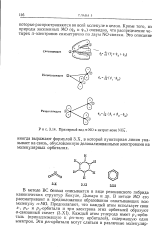 |
Примерный видя - МО в нитрит-ионе М02. [25] |
В методе ВС бензол описывается в виде резонансного гибрида канонических структур Кекуле, Дьюара и др. В методе МО его рассматривают в предположении образования охватывающих всю молекулу я - МО. Каждый атом углерода имеет pz-op 6n - таль ( принадлежащую к ря-типу орбиталей), содержащую один электрон. [26]
Если принять, что все структуры вносят в резонансный гибрид одинаковый вклад, то в случае нафталина 1 2 - и 2 3-связи должны обладать характером двойной связи на 2 / 3 и V3 соответственно. [27]
В теории резонанса считается, что ацетат-ион есть резонансный гибрид двух классических или канонических структур. Каноническая структура представляет собой валентную структуру, удовлетворяющую законам классической теории валентности. [28]
Даже здесь главная структура дает больший вклад в резонансный гибрид, чем остальные формы. [29]
Если принять, что все структуры вносят в резонансный гибрид одинаковый вклад, то в случае нафталина 1 2 - и 2 3-связи должны обладать характером двойной связи на 2 / з и 1 / з соответственно. [30]
Страницы: 1 2 3 4