Двоесвязанный атом
Cтраница 1
 |
Стереохимия соединений азота. [1] |
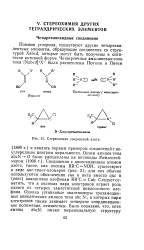
Соединения с двоесвязанным атомом азота, такие, как оксимы RR C NOH, существуют в виде цис-транс-нзомеров ( рис. 21; для них обычно используются обозначения син и анти вместо цис и транс) аналогично олефинам RR C Cab. Следует отметить, что в оксимах пара электронов играет роль одного из четырех заместителей аналогичного оле-фина. Однако устойчивые энантиомеры тризамещен-ных ациклических аминов типа abcN:, в которых пара электронов также занимает четвертое координационное положение, неизвестны. [2]
Дальнейшее увеличение числа двоесвязанных атомов азота приводит к уменьшению основности, хотя резонанс типа ( 76) - ( 77) и продолжает играть свою роль. Одно время считали, что его основный центр находится в имидазольном кольце. Основанием для этого служило то, что пурин является имидазолопирими-дином, а имидазол значительно более основен, чем пиримидин. Однако протон присоединяется к атому азота пиримидинового кольца. Если считать, что сильное электроноакцепторное действие пиримидинового кольца должно влиять на имидазольное кольцо, а затем обратить внимание на р / Са нитробензимидазола как основания ( табл. XVI, стр. ПО), то легко убедиться, как может быть подавлен имидазольный резонанс в пурине. В связи с этим заслуживает внимания то обстоятельство, что пиразольный аналог пурина ( 2, 5, 7-триазаиндол), который способен к увеличивающему основность резонансу ( 76) - ( 77), не является более слабым основанием, чем пурин, хотя пиразол значительно менее основен, чем имидазол. [3]
Даже когда присутствуют несколько двоесвязанных атомов ( а также односвязанный гетероатом, характерный для пятичленного кольца), то сохраняются свойства, связанные с избытком я-электронов. Так, 1 2 3-триазол легко бромируется до 4 5-дибромтриазола; хлор в 3-хлор - 1 2 4-триазоле не вытесняется аминами; 5-амино-тетразол, так же, как 2-аминотиазол, легко диазотируется и сочетается. Таким образом не следует удивляться, если заместители будут придавать разные ионизационные свойства пяти - и шести-членным циклам. [4]
Увеличение кислотных свойств при введении двоесвязанных атомов азота в моноазаиндолы является общим результатом, наиболее ярко проявляющимся в 2, 3, 4, 6-тетраазаиндоле, который по своей кислотности близок к карбоновым кислотам. [5]
Изомерия не ограничивается соединениями, имеющими двоесвязанные атомы углерода, она существует также в соединениях со связями С - N и N - N. Примеры изомерии в таких соединениях приведены ниже. Поскольку химия этих функциональных групп в данной книге детально не рассматривалась, то дальнейшие различия между изомерами описываться не будут. [6]
Заместитель X, будучи другим источником электронов для двоесвязанного атома кислорода, должен оказывать влияние на - М - эффект всей группы. [7]
Гомологи этилена, т.е. алкены, содержащие алкильные группы у двоесвязанных атомов углерода, поглощают при больших длинах волн, чем этилен. Вследствие их индукционного электроноотталкивающего эффекта ( и эффекта гиперконъюгации) алкильные группы увеличивают электронную плотность и, следовательно, возбуждаемость тг-электронов двойной связи. [8]
 |
Геометрическая изомерия диена.| Геометрическая изомерия триена-1 2 3. [9] |
Атом азота с двойной связью может играть ту же роль в геометрической изомерии, что и двоесвязанный атом углерода. [10]
В случае а р-непредельных кислот с более длинной цепью фениль-ная группа не связывается с одним из двоесвязанных атомов углерода, а занимает наиболее удаленное от карбоксильной группы положение ( однако не входит в концевую метильную группу) ( К. Д. Неницеску и И. [11]
Концентрация кислоты может быть тем меньше и температура тем ниже, чем большее число алкильных заместителей у двоесвязанных атомов углерода содержит алкел. В случае этилена необходимы наиболее концентрированная кислота и наиболее высокая температура. Наблюдаемое различие реакционной способности используется для отделения оле-финов в газовом анализе и даже препаративно ( например, для отделения триметил-этилена от изопропилэтилена, см. стр. [12]
В случае a, ( i -непредельных кислот с более длинной цепью фениль-ная группа не связывается с одним из двоесвязанных атомов углерода, а занимает наиболее удаленное от карбоксильной группы положение ( однако не входит в концевую метильную группу) ( К. Д. Неницеску и И. [13]
Метод можно применить только в том случае, когда полярная группа одноатомна или когда направление момента полярной группы совпадает с направлением свяйи между этой группой и двоесвязанным атомом углерода. [14]
Метод можно применить только в том случае, когда полярная группа одноатомна или когда направление момента полярной группы совпадает с направлением связи между этой группой и двоесвязанным атомом углерода. [15]
Страницы: 1 2 3