Кривая - равновесие
Cтраница 4
Кривая равновесия твердое тело - пар в диаграмме р - Т называется кривой сублимации. [46]
Кривая равновесия поднимается над осью Т с ростом температуры. Подъем идет очень круто, в чем можно убедиться, если пренебречь объемом жидкости по сравнению с объемом газа и считать Л мало меняющейся вдоль кривой равновесия, а газ - приближенно идеальным. [47]
Кривая равновесия жидкость - пар ( кривая испарения) может быть определена прибором, изображенным на рисунке 6.2. Очевидно, на кривой испарения крайняя точка со стороны низких температур соответствует температуре отвердевания жидкости под давлением ее насыщающего пара; эту точку называют тройной точкой. [48]
Кривая равновесия жидкость - газ заканчивается в критической точке К, и, как указывалось ранее ( гл. VI), в обход этой точки возможен непрерывный переход от газообразного состояния к жидкому. Твердые тела принципиально отличаются от жидкостей и газов своей анизотропией. Переход между жидкостью и кристаллом не может быть осуществлен непрерывным образом. Именно поэтому для перехода жидкость - твердое тело существование критической точки ( в которой исчезало бы различие между жидкостью и кристаллом) невозможно. [49]
Кривая равновесия для растворов, подчиняющихся закону Рауля, может быть построена следующим образом. [50]
Кривая равновесия и диагональ ограничивают область взаимного существования двух фаз. Выше кривой равновесия расположена область пара, а ниже - область жидкости. [51]
Кривая равновесия строится; обычно по опытным данным, которые для большинства жидкостей можно найти в справочниках физико-химических величин. [52]
Кривая равновесия для растворов, подчиняющихся закону Рауля, может быть построена следующим образом. [53]
Кривая равновесия и диагональ ограничивают область взаимного существования двух фаз. Выше кривой равновесия расположена область пара, а ниже - область жидкости. [54]
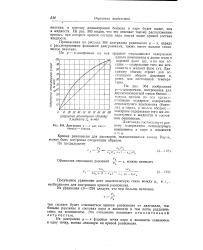 |
Диаграмма у - х для смеси бензол - толуол. [55] |
Кривая равновесия для растворов, подчиняющихся закону Рауля, может быть построена следующим образом. [56]
Кривая равновесия делится на два больших участка: до 650 С - содержание серы увеличивается непрерывно ( хотя н с различной скоростью), а при дальнейшем нагреве оно снижается. [57]
Страницы: 1 2 3 4