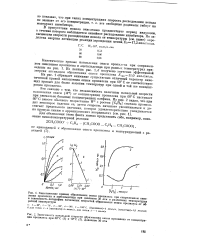
Кинетическая кривая - накопление
Cтраница 2
В качестве иллюстрации на рис. 10 приведена кинетическая кривая накопления этилена и кривая изменения его молярной радиоактивности в реакции крекинга пропана. На рис. 11 приведены вычисленные из этих данных скорости образования и расходования этилена как функция времени. [16]
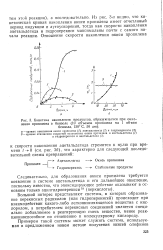 |
Кинетика накопления продуктов, образующихся при окислении пропилена в бензоле ( 10 объемов пропилена на 1 объем бензола, 150 С, 50 am. [17] |
Из рис. 3 а видно, что кинетическая кривая накопления окиси пропилена имеет отчетливый период индукции и аутоускорения, тогда как скорости накопления ацетальдегида и гидроперекиси максимальны почти с самого начала реакции. [18]
На рис. 1 обращает внимание существенно отличный характер кинетической кривой накопления окиси пропилена при 60 С от соответствующих кривых для более высоких температур при одной и той же концентрации пропилена. [20]
По содержанию гидропероксидов в пробах испытуемого топлива строят кинетическую кривую накопления гидропероксидов и по ней находят индукционный период окисления следующим образом. Из точки, соответствующей концентрации гидропероксидов в начальной пробе, проводят прямую, параллельную оси времени. Прямолинейный участок полученной кинетической кривой продолжают вниз до пересечения с этой прямой. Точка пересечения соответствует индукционному периоду. Концентрацию ионола находят по индукционному периоду, пользуясь калибровочным графиком, построенным в координатах период индукции-концентрация ионола. [21]
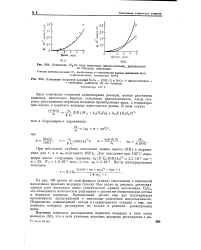 |
А. Изменение W по ходу окисления циклогексанола, рассчитанное. [22] |
Как видно из рисунка, расчетная кривая идет несколько выше кинетической кривой накопления Н202, что объясняется неточностью допущения о равенстве концентраций кетона и перекиси водорода. Проведенный расчет еще раз подтверждает правильность представлений о механизме окисления циклогексанола. Неравенство концентраций кетона и гидроперекиси связано с тем, что перекись водорода расходуется не только в реакции разветвления цепи. [23]
Несколько неожиданным на первый взгляд может показаться то, что кинетическая кривая накопления диметилового эфира триоксиметиленгликоля ( ДЭТГ, п 3) имеет максимум. [24]
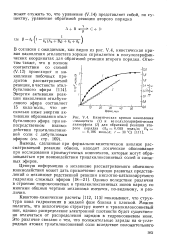 |
Кинетическая кривая накопления. тилацетата ( 1 и ее полулогарифмическая анаморфоза ( 2 для обратимой реакции второго порядка ( А0 0 055 моль / л. В0 0 186 моль / л. C. [25] |
В согласии с ожидаемым, как видно из рис. V.4, кинетическая кривая накопления этилацетата хорошо спрямляется в полулогарифмических координатах для обратимой реакции второго порядка. [26]
В рассмотренном примере необходимо спуститься до столь малых времен, чтобы кинетическая кривая накопления продукта достоверно отклонялась от прямой линии или хотя бы достоверно не была направлена в начало координат. Диапазон значений su нужно подобрать таким, чтобы наклон прямолинейной части кинетической кривой зависел бы OTSU, для чего концентрации не должны быть слишком велики, и в то же время наклон не был бы пропорциональным s0, для чего концентрации не должны быть слишком малы. [27]
Необходимо отметить, что распределение плотностей связей по Y определяет характер кинетической кривой накопления повреждений в материале. [28]
Итак, для действия эндоферментов по механизму неупорядоченной атаки характерной является 5-образная форма кинетической кривой накопления мономера. Такая форма обусловлена постепенным ухудшением связывания фермента с полимерными цепями субстратов по мере уменьшения их степени полимеризации, и поэтому положение точки перегиба на кинетической кривой определяется структурой ( картой) активного центра фермента. [29]
Используя различия в кинетике, авторы предлагают определять компоненты в сложной смеси по линейным участкам изломанной кинетической кривой накопления окрашенного продукта, экстраполируя эти линейные отрезки к начальному моменту времени и используя найденные в однокомпо - нентных смесях константы реакций псевдопервого порядка. [30]
Страницы: 1 2 3 4