Потенциостатическая поляризационная кривая
Cтраница 3
 |
Влияние содержания хрома в стали на предельный ток в области вторичной пассивности в 2 н. хлорной кислоте. [31] |
Известно, что некоторые анионы, в первую очередь, ионы С1, В г и J -, способны вызывать разрушение пассивирующих слоев на отдельных сравнительно небольших участках пассивной поверхности, что нередко приводит к развитию локальной коррозии. Это легко обнаруживается по появлению на потенциостатической поляризационной кривой в области потенциалов между потенциалом пассивации ( ср. [32]
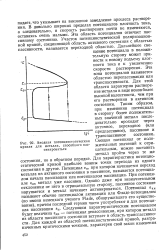 |
Анодная потенциостатическая кривая для металла, способного пассивироваться. [33] |
В довольно широких пределах потенциалов плотность тока, а следовательно, и скорость растворения почти не изменяются, оставаясь очень малыми. Эта область потенциалов отвечает пассивному состоянию. Участок потенциостатической поляризационной кривой, соединяющей область активного состояния с областью пассивности, называется переходной областью. Дальнейшее смещение потенциала в положительную сторону может привести к новому подъему плотности тока и к увеличению скорости растворения. Эта зона потенциалов называется областью перепассивации или транспассивности. Для этой области характерно растворение металла в виде ионов более высокой валентности, чем при его растворении в активном состоянии. Таким образом, при изменении потенциала в сторону более положительных значений металл последовательно проходит через активное, переходное ( или предпассивное), пассивное и транспассивное состояния. [34]
На потенциостатических поляризационных кривых отсутствует область активного анодного растворения. [35]
В случае пассивирующихся металлов большой интерес представляют значения потенциалов границ пассивной области - области высокой коррозионной стойкости - потенциала полной пассивации и потенциала выхода в область перепассивации. Знание этих величин имеет значение не только с теоретической, но и с практической точки зрения, так как позволяет предсказывать коррозионное поведение металлов в зависимости от условий. С этой точки зрения знание потенциостатической поляризационной кривой необходимо для обоснованного подбора корро-зионностойких материалов. [36]
Омическое падение потенциала может быть вызвано аппаратурным оформлением электролизера [18], возникающими или имеющимися на электродах солевыми и окисными пленками, а также зазорами около электрода. Например, только характер границы между электродом и оправкой, определяемый природой и термообработкой армирующего материала, может, согласно [19], изменять ток растворения в пассивном состоянии на два порядка величины. Кроме того, значительные искажения хода потенциостатических поляризационных кривых могут быть обусловлены нарушением при больших плотностях тока изотермичности опытов и возникающими диффузионными ограничениями. [37]
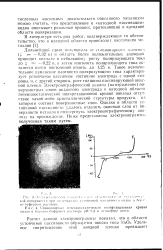 |
Стационариач нотонциосгагическля поляр 1зационная кривая индия и боряпт-пуфс риом pacruope pH.. 3 в атмосфере азота. [38] |
Дальнейший сдвиг покмшиала от стационарною зьаченпм ( т - 0 32 в) в область более положительных значений приводит вначале к небольшому росту поляризующего тока до z - 0 22 и, а затем плотность поляризующего тока останется почти постоянной вплоть до 1 25 в. Такое незначительное изменение плотности поляризующего тока характеризует устойчивое пассивное состояние электрода с одной стороны, и, с другой стороны, рост толщины пассивирующей окис-ной пленки. Электропографический анализ ( на отражение) поверхностных слоев индиевого электрода в катодной области потенциостатической поляризационной кривой показал отсутствие какой-либо кристаллической структуры продукта, из которого состоят поверхностные слои. [39]
Анодные поляризационные кривые можно получать двумя принципиально отличающимися методами. Задавая и поддерживая постоянные значения плотности внешнего тока электрода и замеряя устанавливающиеся при каждой плотности тока значения потенциала электрода получают так называемую гальваностатическую поляризационную кривую. Если, наоборот, поддерживают на электроде постоянные значения потенциала и замеряют устанавливающуюся плотность тока, то получают потенциостатическую поляризационную кривую. Для пассивирующихся электродов упомянутые кривые не вполне идентичны. Поясним это на поляризационной диаграмме. [40]
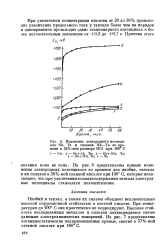
Данные коррозионных испытаний показывают, что в 20 % - ном растворе кислоты совершенно устойчивы сплавы, содержащие не менее 5 вес. Таким образом, при снижении содержания тантала в сплаве ниобий-тантал ниже указанного количества наблюдается заметное увеличение скорости коррозии в растворах соляной кислоты. Потенциостатические поляризационные кривые, представленные на рис. 5, показывают, что ток коррозии сплавов уменьшается по мере увеличения в последних содержания тантала. Анодные поляризационные кривые для сплавов ниобий-тантал занимают промежуточное положение между ниобием и танталом. Эта величина плотности тока характеризует тантал как металл, имеющий высокую химическую стойкость в соляной кислоте. У ниобия ток коррозии в пассивном состоянии в 20 % - ной кислоте равняется 100 мка / см2 ( см. рис. 5 кривая 1), что в пересчете на скорость коррозии будет соответствовать 0 6 г / м2 час. [41]
 |
Изменение электродного потенциала Nb, Та и сплавов Nb-Та во времени в 36 % - ном растворе НС1 при 100 С. [42] |
Ниобий и тантал, а также их сплавы обладают исключительно высокой коррозионной стойкостью в азотной кислоте. При температурах до 100 С они практически не корродируют. Высокая стойкость исследованных металлов и сплавов подтверждается также данными электрохимических измерений. На рис. 7 представлены потенциостатические поляризационные кривые, снятые в 57 % - ной азотной кислоте при 100 С. [43]
Известны два способа их получения: гальваностатический и потенциостатический. Первый сводится к определению потенциала металла при пропусканий между исследуемым металлом и платиновым электродом электрического тока. Получив ряд значений потенциалов для данных плотностей поляризующего тока, строят поляризационную зависимость. При этом фиксируется изменение величины поляризующего тока. В настоящее время для снятия гальваностатических и потенциостатических поляризационных кривых используются специальные приборы - потенциостаты, серийно выпускаемые промышленностью, в которых все операции автоматизированы. Величины, тока или потенциала записываются самописцем. Потенпиоста-чческие зависимости характеризуют кинетику электродных процессов. [44]
Тем более, что и геометрия трещин, как это было установлено ( см. раздел 1), в процессе ее развития изменяется. Это количество электричества может быть определено с помощью интегрирования плотности анодного тока по времени. Внутри труб создавалось давление, формирующее в стенке трубы напряжение, составляющее 0 7 ( Тт. При этом в каждом поддиапазоне изменения потенциалов дожидались установления стационарного значения тока, на что требовалось в условиях опыта до 24 ч на каждую экспериментальную точку, хотя в условиях эксплуатации магистральных газопроводов этот процесс активно-пассивного перехода может быть существенно более длительным. Таким образом была снята потенциостатическая поляризационная кривая, изображенная на рис. 2.3. Потенциалам в интервале минус 1 0 - 0 1 В ( ХСЭ), в конечном итоге, отвечали катодные токи вследствие пассивирующего действия карбонат-бикарбонатной среды. Однако, как это было отмечено выше, при снижении по абсолютной величине потенциала достижению стационарных катодных токов в каждом исследованном поддиапазоне его изменения предшествовало протекание анодного тока. [45]
Страницы: 1 2 3