Анодная кривая
Cтраница 4
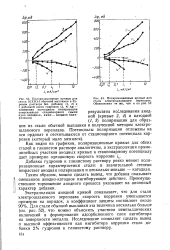
На анодной кривой 2 нелегированното тантала ( рис. 18), напротив, отсутствует область, где он активно растворяется. При легировании ванадия танталом потенциал коррозии сплавов смещается в положительную сторону. Анодные кривые сплавов располагаются между кривыми нелегированных металлов. При этом в зависимости от содержания тантала в сплаве меняется характер кривых. Для сплавов с 50 % тантала и выше на анодных кривых отчетливо проявляется область независимости плотности тока от потенциала. [47]
Характер анодных кривых, в частности величины фп, in, tnn, фпп и Афп, зависит от природы металла и среды. Вместе с тем, скорость растворения хрома в пассивном состоянии примерно на 2 порядка ниже, чем железа. Цирконий в исследованных условиях вообще не проявляет склонности к активному растворению. При анодной поляризации скорость процесса падает до inn 10 - 8 а. [48]
Экстраполяция анодной кривой показывает, что для стали электрошлакового переплава скорость коррозии уменьшается примерно на порядок, а коэффициент защиты составляет около 90 %, Для стали обычной выплавки эта величина несколько больше ( см. рис. 52), что можно объяснить участием неметаллических включений в формировании адсорбционного слоя ингибитора на поверхности металла. Исследование позволяет сделать вывод о высокой эффективности как ингибитора коррозии стали добавки 2 % гудронов к глинистому раствору. [50]
 |
Поляризационные кривые, поясняющие переход металла в пассивное. [51] |
По анодной кривой 1 металл, окисляясь, посылает свои ионы в раствор. Анодная кривая 2 выражает зависимость скорости образования окисла от потенциала, катодная кривая 2 - зависимость скорости восстановления окисла от потенциала; анодная кривая. [52]
На анодной кривой положительное 0 8 В наблюдается участок активации, который, возможно, связан с избирательным травлением карбидов титана в этой области. [53]
Снятие анодных кривых показало, что нержавеющая сталь Х18Н10Т ( рис. 1.26, в, кривая 1) корродирует из активного состояния. [54]
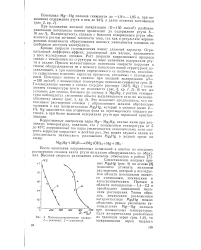 |
Потснциодпнамические кривые. / - реальная. 2 - идеальная. [55] |
Сопоставление анодных кривых Mg3Hg ( рис. 4) на основе [ 8J позволило уточнить механизм растворения, который в исследуемой области потенциалов является смешанным, химическим и электрохимическим. Причем в области потенциалов-1 4 - 2 2 в преобладает химический механизм растворения. [56]
 |
Схематическая поляризационная диаграмма. [57] |
Наклон анодной кривой ( пунктир) показывает смещение потенциала анода в положительном направлении вследствие прохождения тока. Чем круче наклон кривой, тем сильнее поляризуется анод. При больших плотностях тока анодная кривая круто идет вниз. [58]
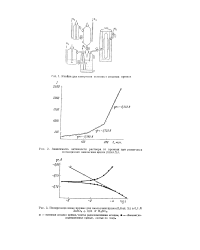 |
Зависимость активности раствора от времени при различных потенциалах амальгамы ципка ( 0 6ат. %.| Поляризационные кривые для амальгамы цинка ( 0 6 ат. % в 0 1. / V. [59] |
О - истинная анодная кривая, снятая радиохимическим методом; - обычные по-ляризационные кривые, снятые по току. [60]
Страницы: 1 2 3 4 5