Кристаллизация - гидрат
Cтраница 1
Кристаллизация гидратов при твердении цемента как в воде, так и в минерализованных средах в нерегулируемых условиях приводит к тому, что образуется ряд твердых растворов новообразований ( в системах СаО - 5Ю2 - Н2О и СаО - А12О3 - Н2О одновременно могут кристаллизоваться до 50 соединений самого различного состава, структуры и свойств), которые из-за их кристал-лохимического подобия невозможно однозначно идентифицировать и выделить для изучения их индивидуальных технологических свойств и областей стабильного существования; без этого ставить вопрос о направленном синтезе цементного камня с заданными свойствами бесполезно. Поэтому на первом этапе работы была поставлена проблема синтеза гидратных фаз ( в том числе монокристаллов с постоянными составом, структурой и свойствами), составляющих камень тампонажных цементов в различных условиях. [1]
Зародыши кристаллизации гидрата легче образуются на свободной поверхности контакта газ - вода. [2]
 |
Структура к ристал - 2 0 А. Структура кристалла. [3] |
Так, при кристаллизации гидрата SOz в атмосфере смеси благородных газов получается осадок, содержащий изоморфно сокрис-таллизованные радон, ксенон и криптон. При этом гелий, неон, аргон остаются в газовой фазе. За счет образования клатратного соединения другого типа можно перевести в осадок и аргон. [4]
Скорость образования зародышей кристаллизации гидрата в значительной степени определяется значением внешнего давления и степенью переохлаждения процесса. С увеличением давления скорость образования зародышей кристаллизации растет. При повышении степени переохлаждения скорость образования зародышей кристаллизации резко возрастет, а, достигнув определенного значения, при заданном давлении плавно снижается. После появления центров кристаллизации гидрат распространяется и занимает всю свободную поверхность контакта газ - вода. Скорость образования сплошной гидратной пленки на поверхности раздела газ - вода зависит от переохлаждения и состояния воды, давления и температуры процесса. Радиальная скорость образования гид-ратной пленки на свободной поверхности вокруг зародышей кристаллизации относительно велика и достигает сотен микрометров в секунду. Она остается постоянной для данных термодинамических условий. С ростом давления, уменьшением удельного объема газа и повышением переохлаждения, т.е. увеличением структурирования воды, скорость образования поверхностно-пленочного гидрата возрастает. [5]
Это соединение получают кристаллизацией гидрата хлорида никеля из пиридина. Таким же способом получают аналогичное соединение железа, растворимое в органических растворителях. [6]
Необходимо отметить еще некоторые особенности кристаллизации гидрата и карбоната кальция. Последними исследованиями при помощи электронного микроскопа было установлено, что частицы гидрата окиси кальция, независимо от способа их получения, имеют шарообразную форму. [7]
Однако, если речь идет о кристаллизации гидратов солей, сопровождающейся сильным увеличением объема твердой фазы, то внутренние напряжения могут быть большими. [8]
Далее от этой точки идет третья ветвь кристаллизации следующего гидрата хлорида стронция. Химический анализ показал, что в соли содержится 36.21 % хлор-иона или 80.97 % хлористого стронция, что близко отвечает шестиводному гидрату. Полученная изотерма растворимости исследуемой системы аналогична диаграмме, установленной предыдущими исследователями. [9]
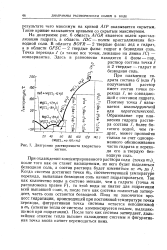 |
Диаграмма растворимости хлористого магния. [10] |
На диаграмме рис. 6 область AJGR является полем кристаллизации гидрата, а область JDC - полем кристаллизации безводной соли. [11]
По достижении этой точки начинается при продолжающемся испарении воды кристаллизация гидрата АХ-иН20, и фигуративная точка раствора направится по кривой bD к точке превращения D, по достижении которой начнется выделение безводной соли АХ и растворение кристаллогидрата АХ-гсН20. [12]
Одним из методов очистки растворов щелочей от хлоридов [72, 73] является кристаллизация гидратов едкого натра и едкого кали. Последние предложения обосновываются диаграммой плавкости, изученной Пикерингом [ 741, а также новыми работами. [13]
При твердении вяжущих на основе гашеной извести протекают два процесса: кристаллизация гидрата окиси кальция и его карбонизация. Кристаллизация идет за счет удаления воды и в этом отношении напоминает изотермическую кристаллизацию с испарением. Она протекает медленно ввиду сравнительно небольших пересыщений раствора. Кристаллы Са ( ОН) 2, срастаясь между собой, образуют известковый каркас. Так как в ходе кристаллизации скорость создания пересыщения за счет испарения воды и скорость кристаллизации постепенно уравновешивают друг друга, образование кристаллов Са ( ОН) 2 некоторое время протекает при постоянном пересыщении. Поскольку процесс испарения протекает медленно, для данного случая характерна небольшая степень пересыщения и, следовательно, очень небольшая скорость кристаллизации. Выше мы упомянули о том, что процесс кристаллизации Са ( ОН) 2 напоминает изотермический процесс образования твердой фазы с испарением. Но на самом деле в начале твердения кристаллизация может идти в неизотермических условиях за счет остатков негашеной извести, гидратация которой связана со значительным тепловым эффектом. [14]
Из протекающих при обычном твердении извести процессов испарение воды, сопровождающееся кристаллизацией гидрата окиси кальция, имеет большее значение, чем карбонизация гидрата окиси кальция. Образующиеся кристаллы последнего срастаются друг с другом, с зернами песка и с кристаллами углекислой извести, образовавшимися на поверхности раствора. Важно также и то обстоятельство, что высыхание вызывает уплотнение студнеобразной массы, а следовательно, и нарастание прочности твердеющих известковых растворов. Преобладающее значение этого процесса при твердении извести подтверждается тем, что испарение воды из известковых растворов происходит значительно быстрее карбонизации. [15]
Страницы: 1 2 3 4