Аффинная лиганда
Cтраница 1
Аффинные лиганды, которые содержат свободные карбоксильные группы, могут быть связаны с ам иноэтилагарозой при помощи водорастворимых карбодиимидов. Этот метод детально обсуждается в разд. [1]
Аффинные лиганды можно присоединять к волокнам также посредством специальных связей, что позволяет освобождать клетки путем химического или ферментативного расщепления этих связей. На рис. 6.17 показано связывание эритроцитов и тимоци-тов на различных волокнах в зависимости от числа молекул кон-канавалина А на 1 см найлонового волокна. [2]
Высокомолекулярные аффинные лиганды обычно открывают больше возможностей для приготовления аффинных сорбентов. Ряд очень активных аффинных сорбентов получен при прямом присоединении белка к нерастворимому носителю ( многочисленные примеры приведены в гл. Однако в этом случае очень важным является условие, чтобы присоединение белка к нерастворимому носителю не приводило к изменению его натив-ной конформации. [3]
Иммобилизованные аффинные лиганды, которые поглощают свет при 260 нм, можно определять, спектрофотометрируя непосредственно модифицированные гели. Гель суспендируют в оптически чистом полиакриламиде, зтиленгликоле или глицерине и определяют оптическую плотность в кюветах толщиной 1 мм относительно немодифицированного геля в двулучевом спектрофотометре. [4]
В этот обзор включены также аффинные лиганды с очень узкой специфичностью. Например, если к носителю прикрепить ингибитор, специфичный для единственного фермента, образующийся сорбент также будет специфичен только для данного фермента. Однако для использования специфических лигандов необходимо проводить различные и часто очень трудоемкие синтезы сорбента для каждого разделения. Не все аффинанты, которые подходят для комплементарного связывания макромолекул, имеют также подходящие функциональные группы для их прикрепления к нерастворимому носителю. Очевидно, что матрица с групповой специфичностью, содержащая общий лиганд, проявляет аффинность к большой группе биологических макромолекул. [5]
Очевидно, что присутствие в иммобилизованных аффинных лигандах примесей, обладающих таким же или более сильным сродством к выделяемым молекулам, может ухудшать полезность специфического сорбента при градиентных разделениях. [6]
Диметилформамиа требуется для растворения эстрадиола; если аффинные лиганды растворимы в воде, в нем нет необходимости. Замещенную сефарозу переносят в колонку и промывают 50 % - ным водным раствором диметилформамида до отсутствия радиоактивности в элюате. Рекомендуется для промывания использовать 10 л раствора и проводить его в течение 3 - 5 дней. По этой методике 1 мл влажной сефарозы может связать - 0 5 мкмоля эстрадиола. [7]
Во многих случаях для связывания с нерастворимыми носителями использовались аффинные лиганды, меченные радиоактивными изотопами. Связанный аффинный лиганд легко определяется на основе измерения радиоактивности. Например, Грин и Соме [30] определили таким образом количество биотина, связанного с сефарозой. [8]
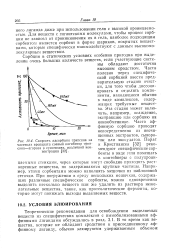 |
Скорость адсорбции трипсина на частицах препарата соевый ингибитор трипсина-агароза в суспензиях, различной концентрации. [9] |
Теоретические рекомендации для освобождения выделяемых веществ из специфических комплексов с иммобилизованными аффинными лигандами обсуждались в разд. [10]
Количество исследований, в которых в качестве нерастворимого носителя применяется агароза и ее производные с привитыми аффинными лигандами, увеличивается по мере развития аффинной хроматографии, и полный обзор таких работ в рамках одной главы практически невозможен. Так, в 1968 г. были опубликованы всего две работы, описывающие использование агарозы в качестве носителя в аффинной хроматографии, в 1969 г. таких работ было уже примерно 10, а в 1970 г. - около 20, а в 1971 г. - более 40, в 1972 г. - более 70, а в последующие годы это число было вновь превышено. В табл. 7.3 приведены некоторые примеры использования агарозы в аффинной хроматографии, показывающие возможности этого метода. [11]
Достаточная проницаемость нерастворимого носителя необходима для того, чтобы не затруднялось образование комплексов макромолекул с комплементарными аффинными лигандами; этот вопрос детально уже обсуждался в разд. Концентрация присоединенного аффинного лиганда, легко доступного для выделяемого вещества, в этом случае должна быть очень высока, для того чтобы достичь сильного взаимодействия, которое физически задерживает выделяемые вещества, мигрирующие по колонке. [12]
Носители должны обладать достаточным числам химических групп, которые могут быть активированы или модифицированы таким образом, чтобы приобрести способность связывать аффинные лиганды. Емкость специфического сорбента, приготовленного присоединением аффинного лиганда к нерастворимому носителю, зависит от числа этих групп. [13]
Специфические сорбенты, использующие исключительные свойства биологически активных веществ образовывать специфические и обратимые комплексы, в огромной степени облегчают выделение ряда ферментов, их ингибиторов и кофакторов, антител и антигенов, лектинов, гликопротеинов, гликополисахаридов, нуклеиновых кислот, нуклеотидов, жиров, транспортных и рецепторных белков, гормонов и их рецепторов, клеток и многих других соединений, как это представлено в обзорной табл. 11.1. Наряду с названием выделяемого вещества в таблице приведены также используемые аффинные лиганды, нерастворимые носители и пространственные труппы, причем указано, аффинный лиганд или нерастворимая матрица модифицированы данной пространственной группой. Обзорная таблица включает выделения веществ как с помощью типичной биоаффинной хроматографии, так и с помощью гидрофобной или ковалентной хроматографии. [14]
Наиболее широко используемый метод связывания аффинного лиганда с сефарозой разработан Поратом, Аксеном и Эрнбаком [2,55]; он основан на активации носителя бромцианом. Аффинные лиганды связываются посредством первичных алифатических или ароматических аминогрупп в непротонированной форме. Ак-сен и Эрнбак [1] предположили, что при этом образуются три различные структуры, а именно N-замещенные карбаматы, N-за-мещенпые имидокарбонаты и N-замещенные изомочевины. N-за-мещенная мочевина, как предположил Свенсон [72] на основании работ по изоэлектрофокусированию, является преобладающей формой. [15]
Страницы: 1 2 3