3-диоксан
Cтраница 3
Исследование взаимодействия алкил-1 3-диоксанов с различными замещенными фенолами ( табл. 4) показывает, что образование диена эффективно протекает при использовании фенолов, не содержащих наиболее активных а-водородных атомов, например, 2 6-ди - ( грет-бу-тил) фенола. [31]
Важная роль 1 3-диоксанов и родственных 1 3 2-гетероциклов в тонком органическом синтезе является одной из причин неослабевающего интереса к особенностям строения и вопросам конформацион-ного анализа гетероаналогов циклогексана. [32]
Исследовано влияние 1 3-диоксанов и сложных моноэфиров гликолей на количество форменных элементов в 1 мм3 гемолимфы. Установлено изменение этого показателя, как ответная реакция моллюска на токсическое действие изученных соединений. [33]
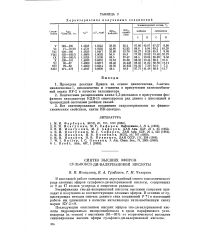 |
Характеристика полученных соединений. [34] |
Контактным расщеплением алкил-1 3-диоксанов в присутствии фосфатного катализатора КДВ-15 синтезирован ряд диенов с циссоидной и трансоидной системами двойных связей. [35]
В 5-алкилзамещенных 1 3-диоксанах заместитель в положении 5 гораздо менее склонен занимать экваториальное положение, чем заместитель в производных циклогексана [184], и величина - AG намного ниже. [36]
Из пропана получить 1 3-диоксан. [37]
В настоящее время 1 3-диоксаны испытаны в различных областях, часть из них зарекомендовала себя как эффективные растворители-и эластомеры Некоторые проявляют антигистамннную и спазмолитическую, активность. Получение замещенных 1 3-диоксанов на основе моновиниловых эфиров первично-третичных гликолей позволяет вводить различные заместители в диоксановый цикл, что значительно может расширить сферу их практического использования. [38]
Таким образом, 1 3-диоксаны с б-алкоксиэтиловым радикалом в молекуле оказываются менее активными, чем соответствующие алкилзамещенные 1 3-диоксаны. [39]
Исследование соединений ряда 1 3-диоксана проводится в значительно меньшей степени, чем изучение 1 4-диоксана и родственных ему соединений, которое становится все более интенсивным. Это легко может быть объяснено тем фактом, что 1 4-диоксан уже около двадцати лет является продуктом многотоннажного промышленного производства, в то время как применение изомерного 1 3-диоксана еще ждет промышленного развития. [40]
Каталитический пиролиз алкилированных 1 3-диоксанов над дегидратирующими катализаторами приводит к получению алифатических диолефинов с хорошими выходами. При этом в качестве разбавителей обычно применяют азот или пар, способствующие удалению воды. В аналогичных условиях из 2 4-диметил - 1 3-диоксана образуется изопрен. Эта реакция удобна для получения определенных диолефинов в относительно чистом состоянии. [41]
Единственным моноалкильным производным 1 3-диоксана, полученным Бейкером [114] по реакции Принса, является 4-метильное соединение: конденсация пропилена с параформальдегидом проводилась в присутствии ледяной уксусной и серной кислот. Вполне возможно, что 1 3-диоксаны с более тяжелыми алкильными группами могут быть получены при помощи той же реакции, исходя из а-алкенов большего молекулярного веса. [42]
Общим методом синтеза 1 3-диоксанов с галогеном в боковой цепи является взаимодействие галогенальдегидов с гликолями. [43]
Исследование соединений ряда 1 3-диоксана проводится в значительно меньшей степени, чем изучение 1 4-диоксана и родственных ему соединений, которое становится все более интенсивным. Это легко может быть объяснено тем фактом, что 1 4-диоксан уже около двадцати лет является продуктом многотоннажного промышленного производства, в то время как применение изомерного 1 3-диоксана еще ждет промышленного развития. [44]
Каталитический пиролиз алкилированных 1 3-диоксанов над дегидратирующими катализаторами приводит к получению алифатических диолефинов с хорошими выходами. При этом в качестве разбавителей обычно применяют азот или пар, способствующие удалению воды. В аналогичных условиях из 2 4-диметил - 1 3-диоксана образуется изопрен. Эта реакция удобна для получения определенных диолефинов в относительно чистом состоянии. [45]
Страницы: 1 2 3 4