Пентафторфенол
Cтраница 1
Пентафторфенол следует хранить в темноте в плотно закрытом и за пара финенном стеклянном или полиэтиленовом сосуде. [1]
КОН дает пентафторфенол, с МНз - пентафтор-анилин. [2]
Результаты исследования реакций пентафторфенола и - тиофе-нола с тетрафторэтиленом и бромом позволяют также высказать предположение о большей предпочтительности взаимодействия дифторкарбена со связью С - О и С - S, чем со связью С - F пентафторфенола и - тиофенола. Если бы процесс внедрения: CF2 по связи С - F имел место в заметной степени, то среди продуктов реакций могли оказаться ожидаемые n - трифторметильные производные гептафторбензилбромида и перфторбензилфенилового эфира. [3]
По аналогии с превращением пентафторфенола под действием тетра-фторэтилена в перфториндан можно представить и протекание этой реакции. В пользу участия в ней а-хлоргексафтор - и гепта-фторбензильных радикалов свидетельствуют данные по взаимодействию пентафторфенола с 1, 2-дибромхлортрифторэтаном. [4]
При синтезе первых мономеров используют пентафторфенол и октафтор-изобутилен - [19] или гексафторпропиленоксид ( пат. Описан, в частности, терполимер ТФЭ, перфторалкилвинилового эфира и перфтор-феноксиизопропилвинилового эфира ( пат. Один из путей синтеза циансодержащего мономера состоит в реакции перфтор-а-цианпро-пионилфторида с гексафторпропиленоксидом и последующем пиролизе продукта реакции с карбонатом натрия ( пат. [5]
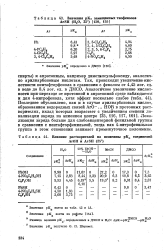 |
Значения рКа замещенных тиофенолов ArSH ( Н20, 25.| Влияние растворителей на величины рК0 соединений. [6] |
Так, происходит увеличение кислотности пентафторфенола в сравнении с фенолом от 4 45 лог. Локализация заряда больше для слабоакцепторной фенильной группы в сравнении с пентафторфенильнбй, тогда как 4-нитрофенильная группа в этом отношении занимает промежуточное положение. [7]
Легко реагирует с азотной кислотой и пентафторфенол. [8]
Паммеру удалось также получить полиоксиперфторфенилены взаимодействием пентафторфенола с водным раствором едкого кали. [9]
В большинстве методов синтеза полиперфторфениленовых эфиров используется пентафторфенол или его соли. Эти методы во многих отношениях аналогичны методам синтеза обычных [94], а также некоторых частично фторированных полиарильных эфиров [95-97] по реакции Ульмана. [10]
Раствор 5 ммоль трвт-бутвлокоикарбоналаминокислоты и 5 5 ммоль пентафторфенола в 5 мл сухого этилацегата или омеок диокоав - ДМФА охлаждают до О С и при размешивании вносят 5 5 ммоль ДЦГК в 5 мл этияацетата. Реакционную омеоь перемешивают 4 ч при О С, дицикло-гексилмочевину отфильтровывают, раотворитель удаляют в вакууме, а остаток растирают о гекоаном и крноталлизуют жз подходящего рао-творителя. [11]
В пользу этого предположения свидетельствуют данные по со-пиролизу пентафторфенола [79] и - тиофенола [15] с тетрафторэтиленом в присутствии брома, приводящему к образованию геп-тафторбензилбромида ( ср. Аналогичный процесс протекает и с 1, 2-дибромтетрафторэта-ном, который в условиях реакции способен дебромироваться с образованием тетрафторэтилена. [12]
 |
Строение и свойства пе, Э - флуорешшлетилокоикарбонидаминокислот. [13] |
К раствору 2 ммоль Лям-аминокислоты я 2 ммоль пентафторфенола в оухом диокоане, этилацетате или в оыеож одного иэ них с ДЮА ( 5 - 10 мл) добавляют при охлаждении до О С и перемешивании 2 ииоль ЛДГК. Дициклогекмшючевину отфильтровывают, растворитель отгоняют на роторном испарителе при 40 С, а оота-ток растирают о гекоаном. Затвердевший продукт отфильтровывают и криоталлизуюТ из подходящего раотворителя. [14]
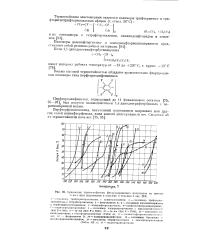 |
Сраннснпе термостойкости фторсодержащнх полимеров по потере. [15] |
Страницы: 1 2 3