Углеводородный заместитель
Cтраница 3
При увеличении числа и ( или) длины углеводородных заместителей в алкилбензолах эта положительная адсорбция на полярном адсорбенте из водных растворов усиливается, так что возможно их разделение в порядке роста числа атомов углерода в молекуле. На рис. 16.13 показана Хроматограмма водных растворов полиметил - и моно-н-алкилбензолов на силикагеле с гидроксилированной поверхностью в порядке увеличения углеводородной части молекулы. [31]
Отличительной особенностью радиационно-химического метода является высокая чувствительность к углеводородным заместителям в основной цепи, что, в частности, позволяет уверенно отличать полиэтилены высокого и низкого давления. [32]
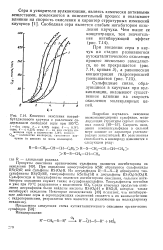 |
Кинетика окисления натрий-бутадиенового каучука с различным содержанием свободной серы при 100 С. [33] |
Скорость окисления алкенилсульфидов в сильной мере зависит от характера углеводородных заместителей. [34]
Соединения, в которых карбонильная группа связана с двумя углеводородными заместителями, одинаковыми или различными, называют кетонами. [35]
Для стабилизации полимеров рекомендованы гидразин и его продукты замещения, содержащие углеводородные заместители, соли гидразина, гидразиды кислот ( ацилированные производные гидразина), гидразоны и азины оксосоединений. [36]
Предполагается, что утяжеление молекулы мономера, обусловленное увеличением длины углеводородного заместителя, приводит к снижению kp и усилению стереоконтроля поверхностью характера присоединения мономера в актах роста цепей. [37]
Меркаптаны ( тиолы) имеют строение RSH, где R - углеводородный заместитель всех типов ( алканов, цикланов, аренов, гибридных) разной молекулярной массы. Температура кипения индивидуальных алкилмеркаптанов Cj-Сб составляет при атмосферном давлении 6 - 140 С. Они обладают сильно неприятным запахом. Это свойство их используется в практике газоснабжения городов и сел для предупреждения о неисправности газовой линии. В качестве одоранта бытовых газов используется этилмеркаптан. [38]
Меркаптаны ( тиолы) имеют строение RSH, где R - углеводородный заместитель всех типов ( алканов, цикланов, аренов, гибридных) разной молекулярной массы. Температура кипения индивидуальных алкилмеркаптанов С, - С6 составляет при атмосферном давлении 6 - 140 С. Они обладают сильно неприятным запахом. Это свойство их используется в практике газоснабжения городов и сел для предупреждения о неисправности газовой линии. В качестве одоранта бытовых Тазов используется этилмеркаптан. [39]
Меркаптаны ( тиолы) имеют строение RSH, где R - углеводородный заместитель всех типов ( алканов, цикланов, аренов, гибридных) разной молекулярной массы. Температура кипения индивидуальных алкилмеркаптанов С, - С6 составляет при атмосферном давлении 6 - 140 С. Они обладают сильно неприятным запахом. Это свойство их используется в практике газоснабжения городов и сел для предупреждения о неисправности газовой линии. В качестве одоранта бытовых газов используется этилмеркаптан. [40]
Меркаптаны ( тиолы) имеют строение RSH, где R - углеводородный заместитель всех типов ( алканов, цикланов, аренов, гибридных) разной молекулярной массы. Они обладают сильно неприятным запахом. Это свойство их используется в практике газоснабжения городов и сел для предупреждения о неисправности газовой линии. В качестве одоранта бытовых газов используется этилмеркаптан. [41]
К обратному эффекту - к снижению взаимодействия между цепями - приводят боковые углеводородные заместители. [42]
Из изложенного в данном разделе очевидно, что при увеличении числа углеводородных заместителей при реакционном центре диссоциация должна облегчаться за счет действия как электронных, так и стерических факторов. Поэтому реакции мономолекулярного замещения особенно характерны для третичных систем. [43]
Из экспериментальных данных следует, что индукционные постоянные водорода и всех насыщенных углеводородных заместителей, содержащих углеродные атомы только в первом валентном состоянии, представляют собой обособленную шкалу, которая при строгом подходе не является единым целым с совокупностью величин а для всех остальных заместителей. Правда, при решении практических задач этим часто можно пренебречь. [44]
Атом олова также имеет тригонально-бипирамидальную координацию ( рис. 17) с углеводородными заместителями в экваториальных положениях ( Sn - С 2 16А, ( ср. Sn-N ( 2 62 А) в этой структуре значительно длиннее, чем в Me3SnNCS, а расстояние Sn-S ( 2 58А), напротив, значительно короче и лишь на 0 15 А превышает длину ординарной ковалентной связи. S-производным, хотя отмеченное выше удли - 1нение связи Sn-S и укорочение связи S-С до 1 71 А по сравнению с 1 78 А в Ph3SnSC6H2Me3 [101] указывают на некоторый вклад тиопиридоновой формы. [45]
Страницы: 1 2 3 4