Зарождение - свободный радикал
Cтраница 2
Следовательно, ингибитор расходуется в окисляющемся циклогексане только в результате реакции со свободными радикалами [11], и скорость его расходования должна быть пропорциональна скорости зарождения свободных радикалов. С одной молекулой фенола или нафтола обычно реагируют в реакции окисления два свободных радикала [11], поэтому скорость инициирования цепей в реакции равна удвоенной скорости расходования ингибитора. [17]
Самоускоренное течение процесса окисления, иначе называемое автокаталитическим, при низких температурах ( до 130 - 150 С) объясняется накоплением в окисляющемся веществе гидроперо-ксидных групп, распад которых приводит к добавочному зарождению свободных радикалов - вырожденному разветвлению цепи. [19]
Иногда, например в случае этилена, инициирование может осуществляться термическим путем, при этом образуется бирадикал - СН2 - СН2 - - В случае винилацетата инициирование полимеризации чаще всего осуществляется при зарождении свободных радикалов под действием света, что дает возможность проводить полимеризацию при обычных температурах. Реакция полимеризации может начаться с внедрения в мономер свободного радикала; так, полимеризацию винилацетата могут индуцировать атомы водорода и метальные радикалы. Катализированную полимеризацию можно осуществить с помощью кислорода и перекисей; последние легко образуют свободные радикалы, распадаясь по связи О - О. [20]
Если реакция обрыва определяется реакцией только одного радикала, то в стационарном состоянии, когда скорость зарождения цепи равна скорости обрыва, при линейном обрыве концентрация свободных радикалов будет прямо пропорциональна скорости зарождения цепи, а при квадратичном обрыве концентрация свободных радикалов будет прямо пропорциональна корню квадратному из скорости зарождения свободных радикалов. [21]
Если реакция обрыва определяется реакцией только одного радикала, то в стационарном состоянии, когда скорость зарождения цепи равна скорости обрыва, при линейном обрыве концентрация свободных радикалов будет прямо пропорциональна скорости зарождения цепи, а при квадратичном обрыве концентрация свободных радикалов будет прямо пропорциональна корню квадратному из скорости зарождения свободных радикалов. [22]
Явлению выхода гетер огенно-каталитнческих реакций в жидкой фазе в объем, характерному для реакций окисления, посвящено значительное количество исследований. Обосновывается механизм зарождения свободных радикалов на поверхности оксидов металлов. На примере окисления пропанола на платине дается оценка доли объемной и поверхностной ( 30 %) реакций образования альдегида. Показана возможность ингибировання объемного продолжения каталитической реакции растворимыми или твердыми ингибиторами. [23]
При импульсном фотолизе смесей одного из указанных выше гидридов с кислородом, во всех случаях наблюдается либо взрывная, либо медленная реакция. Это обусловливается зарождением свободных радикалов, инициирующих цепные реакции окисления в условиях высокой температуры, получающейся в результате импульсного нагревания. Воспламенение имеет резко выраженные пределы, которые, как и следовало ожидать, зависят от интенсивности инициирующего импульса. Это обстоятельство дает возможность фотографировать спектры поглощения промежуточных веществ как перед взрывом, так и после него. [24]
Она максимальна для 3 06 - 10 - 2 моль / л стеарата марганца. Это объясняется высокой / скоростью зарождения свободных радикалов, образующихся как при непосредственном ускорении распада алкилгидроперекисей, так и в основном при взаимодействии радикала ROO с марганцем. [25]
В [3.5] показано, что в условиях термического разложения при отсутствии кислорода образование свободных радикалов идет в основном по мономолекулярной реакции. Там же предложена новая теория зарождения свободных радикалов при окислении в объеме жидких углеводородов. [26]
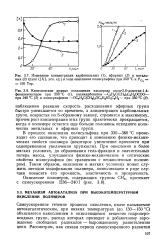
Изучение спектров поглощения реакционных растворов окисления n - ксилола, содержащих а-нафтол, показывает, что переход двухвалентного кобальта в трехвалентное состояние наблюдается после израсходования ингибитора. Это свидетельствует о том, что зарождение свободных радикалов происходит без валентного превращения кобальта. [27]
Изучение спектров поглощения реакционных растворов окисления я-ксилола, содержащих а-нафтол, показывает, что переход двухвалентного кобальта в трехвалентное состояние наблюдается после израсходования ингибитора. Это свидетельствует о том, что зарождение свободных радикалов происходит без валентного превращения кобальта. [28]
Изучение спектров поглощения реакционных растворов окисления п-ксилола, содержащих oL - нафтол, показало, что переход двухвалентного кобальта в трехвалентное состояние наблюдается после израсходования ингибитора. Это свидетельствует о том, что зарождение свободных радикалов происходит без валентного превращения кобальта. [29]
Первичное зарождение свободного радикала представляет собой процесс, в результате которого появляющаяся свободная валентность возникает наново, а не взамен исчезнувшей, как это происходит в ходе реакции продолжения цепи. Выше уже указывалось, что такое зарождение свободных радикалов происходит либо из исходных веществ ( при термическом распаде одного из них или при взаимодействии их между собой) либо при актах разветвления. [30]
Страницы: 1 2 3