Заряд - анион
Cтраница 3
В трилонате хрома элементарным анализом определялось содержание С и Н и устанавливался заряд аниона CrY - фильтрованием через анионит, взятый в Cl-форме, и титрованием фильтрата ( НС1) щелочью с индикатором метилоранжем. [31]
Однако такой подход приводит к некоторым затруднениям, поскольку часть пространства между зарядами анионов занята молекулами двухосновной кислоты, а не растворителем. [32]
Это правило - не что иное, как непосредственное применение принципа Полинга [119]: заряд аниона равен сумме электростатических сил тех связей, которые он образует с соседними катионами. Такое же правило имеет место для катиона. [33]
При составлении этих выражений надо помнить, что сумма зарядов катионов должна равняться сумме зарядов анионов. [34]
Очевидно, что эти продукты лишены антихолинэстеразной активности из-за выраженного нуклеофильного эффекта, осуществляемого зарядом аниона. Таким образом, гидролиз почти всегда приводит к полной детоксикации вещества. Дальнейшее разрушение этих первичных продуктов гидролиза уже не представляет интереса для токсикологии. [35]
Для золя Fe ( OH) 3, частицы которого заряжены положительно, имеет значение заряд аниона, входящего в состав электролита-коагулятора. [36]
А - постоянная, зависящая от температуры и диэлектрической проницаемости; га, ZK - заряды аниона и катиона соответственно. Средний ионный коэффициент активности j определяется экспериментально. [37]
В результате происходит детоксикация соединения, так как образующиеся вещества имеют анионную природу, а заряд аниона препятствует взаимодействию с холинэстеразой. Эта реакция наиболее быстро протекает в организме человека и теплокровных животных и в ряде случаев определяет избирательность действия инсектицидов. [38]
 |
Названия родоначальных оксокислот фосфора и мышьяка. [39] |
Степень окисления металла при необходимости может быть указана по системе Штока либо выражена в виде заряда аниона по системе Эвенса-Бассета ( см. с. Давно существующее окончание ид для карбанионов ( например: NaCH3 метанид натрия) принято в правилах IUPAC в разделе С [5], но не в разделе D [1] 1 В последнем из этих разделов имеются, однако, такие названия, как диэтилфосфид калия для КР ( С2Н5) г. Название ацетилид натрия для NaC CH используется IUPAC и СА; приемлемым является также название эти-нилнатрий. [40]
На устойчивость аммиакатов солей с одним и тем же центральным ионом существенное влияние оказывают величина и заряд анионов, находящихся во внешней сфере. При учете одних только электростатических сил можно было бы сделать вывод о том, что с уменьшением заряда и увеличением размера внешних анионов устойчивость комплексных аммиакатов должна возрастать. Подобные ряды устойчивости аммиакатов действительно наблюдаются в случае галогенидов некоторых металлов и известны под названием нормальных рядов устойчивости. [41]
Величина ks сильно зависит от природы иона металла, но она почти не чувствует природу и заряд аниона; действительно, ее величина почти одна и та же и для входящего иона, и для незаряженного лиганда. Первое следствие этой картины состоит в том, что k близка по величине к константе скорости обмена растворителя между объемом и первичной сольватной оболочкой ( гл. [42]
Для золя Ре ( ОН) з, частицы которого обычно заряжены положительно, имеет значение заряд аниона, входящего в состав электролита-коагулянта. [43]
При диссоциации многоосновных кислот каждый последующий ион водорода отщепляется труднее, чем предыдущий, из-за возрастания заряда аниона, притяжение которого ему приходится преодолевать. [44]
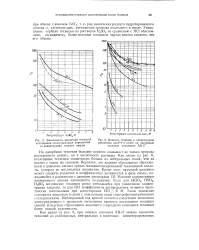 |
Зависимость адсорбции технеция.| Влияние природы и концентрации. [45] |
Страницы: 1 2 3 4