Небольшой положительный заряд
Cтраница 1
Небольшой положительный заряд ( менее 0 04) локализован и на атомах водорода. [1]
 |
Структура грозового облака. [2] |
В нижней части облака скапливается небольшой положительный заряд. В основной части облака сосредоточены отрицательно заряженные частицы. Основание этой части находится, примерно, на 1 км выше видимого основания облака, а высота может достигать 6 км. В верхней части облака сосредоточены положительные ааряды. Такое облако, несущее заряды обоих знаков, называется биполярным. [3]
Снова на атоме углерода сосредоточен небольшой положительный заряд, однако распределение отрицательного заряда между атомами серы и азота существенно иное. [4]
 |
Бинарные соединения углерода и их значения ДО, 298 ( кДж / моль. [5] |
Хотя все четыре атома водорода несут небольшие положительные заряды ( - 0 065 элементарного заряда), их расположение в вершинах тетраэдра приводит к отсутствию у СН4 электрического дипольного момента. Средняя энергия связей С - Н велика и составляет 415 кДж / моль. [6]
Атом водорода, наоборот, приобретает небольшой положительный заряд б и может взаимодействовать с неподеленными парами электронов атома кислорода соседней молекулы воды. [7]
Спрашивается, какую силу испытает на себе небольшой положительный заряд, находящийся в точке А. [8]
При рН 3 5 гуанин несет в среднем лишь небольшой положительный заряд, который не может компенсировать вклад отрицательного заряда фосфорной кислоты. Иное дело - в случае присоединения остатка цитидиловой кислоты. Это означает, что присоединение цитидилового звена практически не изменяет заряд фрагмента, в то время как его сечение увеличивается. [9]
Далее КО и SO3 соединяются в KOSO3, обладающее еще небольшим положительным зарядом. Аналогично можно представить себе возникновение сернокислого алюминия A1203 ( SO3) 3, с той лишь разницей, что это соединение в небольшой мере электроотрицательно. Образование же двойной соли KOSO3 - f - Al O3 ( SO3) g легко объясняется соединением обеих противоположно заряженных составных частей - сернокислого калия и сернокислого алюминия. [10]
При этом большая часть частиц при взаимодействии с жидкой средой приобретает небольшой положительный заряд и передвигается к катоду, который быстро покрывается толстым слоем рыхлых агрегатов частиц. Анод, вначале чистый, затем покрывается частицами, которые переносятся с катода. С течением времени все межэлектродное пространство заполняется агрегатами частиц и при определенной напряженности поля происходит пробой за счет образования мостика с малым сопротивлением, который соединяет электроды. С увеличением диэлектрической проницаемости жидкого диэлектрика сопротивление мостиков уменьшается, что обусловлено различной степенью агрегации частиц в различных средах. [11]
 |
Структура и полярность некоторых молекул.| Модель ион-диполъной связи. [12] |
ЭСО: связи СО полярны, причем на атоме углерода находится небольшой положительный заряд, а на каждом из атомов кислорода-такой же отрицательный заряд. Ясно, что центр положительного заряда молекулы сосредоточен на атоме углерода, однако и центр отрицательного заряда в данном случае также приходится на углерод, поскольку оба атома кислорода расположены по обе стороны от углерода на одной прямой и на равном расстоянии. Таким образом, несмотря на то что диоксид углерода имеет полярные связи, он оказывается неполярной молекулой, и причиной этого является ее линейное строение. Однако линейная молекула SCO: полярна, поскольку связи С - S и С - О имеют различную длину и различную полярность. В общем случае, если атомы или группы атомов, присоединенные к центральному атому, идентичны или расположены симметрично относительно него ( образуя, например, линейную, плоскую треугольную, те-траэдрическую и т.п. структуру), молекула оказывается неполярной. Молекулы, в которых к центральному атому присоединены неодинаковые группы, или молекулы с несимметричным расположением групп, полярны. На рис. 8.14 изображены некоторые примеры полярных и неполярных молекул. [13]
В результате перераспределения электронной плотности при образовании ст-связей и я-дативных связей может возникать небольшой положительный заряд на атоме хрома. Координационное число определяется числом вакантных 3d - и 4р - орбиталей атома хрома в состоянии, когда все одиночные электроны спарены. [14]
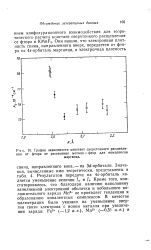 |
График зависимости констант сверхтонкого расщепления от фтора от расстояния металл - фтор для комплексов. [15] |
Страницы: 1 2 3 4