Большой отрицательный заряд
Cтраница 3
Характерным для всех трех веществ является резкое падение ингибирующей способности с увеличением Дк. Это объясняется десорбцией органических анионов с поверхности катода при приобретении ею достаточно большого отрицательного заряда. [31]
Более сложная картина наблюдается для ароматических и гетероциклических соединений, адсорбция которых может сопровождаться л-электронным взаимодействием с поверхностью металла. Такому взаимодействию естественно благоприятствует наличие положительных зарядов на поверхности электрода и, наоборот, при достаточно большом отрицательном заряде поверхности в результате отталкивания л-электронов происходит изменение ориентации адсорбированных органических молекул. Таким образом, поверхностная активность органических веществ, молекулы которых обладают системой сопряженных л-электронных связей, характеризуется наличием двух адсорбционных состояний. Эту особенность и отражает кривая 3 на рис. 2.7, состоящая из двух участков, каждый из которых дает зависимость - АС от Е для соответствующей ориентации молекул адсорбата. [32]
В начале все амфолиты распределены равномерно по объему колонки. При подключении электрического тока амфолиты, имеющие изоэлектрические точки при кислых значениях рН и располагающиеся у катода, депротонируются, приобретают большой отрицательный заряд и начинают двигаться к аноду. В то же время амфолиты, расположенные около анода и имеющие изоэлектрические точки при щелочных значениях рН, протонируются, приобретают положительный заряд и движутся к катоду. Вследствие этого по мере приближения к электродам все амфолиты проходят такую область геля, где рН оказывается равным изоэлектрической точке амфолитов. В этой области суммарный заряд амфолитов становится равным нулю и они перестают передвигаться к электродам. Накопление амфолитов, обладающих одним и тем же pi, в одной зоне приводит к созданию мощного буфера, способного поддерживать рН, равный изоэлектрической точке этой группы амфолитов. Если формирование градиента рНпроисходит в присутствии белка, суммарный заряд молекулы которого определяется соотношением кислых и щелочных аминокислот, или если белок наносят на уже сформированный градиент рН, то молекулы белка ведут себя так же, как и молекулы амфолитов. Вследствие этого после окончания процесса изоэлектрофокусирования белки концентрируются в виде очень узких зон, положение которых определяется изоэлектрической точкой белка. [33]
Однако для комплекса, образованного ионом металла с координационным числом 6, предполагаемая отдача шести пар электронов центральному иону сомнительна в связи с накоплением очень большого отрицательного заряда на атоме металла. Хотя мы и хотели бы сохранить простоту модели Сиджвика, необходимо признать, что она требует усовершенствования не только из-за возражений, на которые мы только что указывали, но и по ряду других причин, которые станут очевидны ниже. [34]
Подобное простое описание страдает двумя недостатками. Во-первых, образование четырех дативных кова-лентных связей приводит к появлению на атоме никеля формального заряда - 4, и даже при неодинаковом обобществлении электронов атом никеля неизбежно должен внести довольно большой отрицательный заряд. [35]
В связи с тем что сетка расположена близко к катоду ( ближе, чем анод), влияние сеточного напряжения на анодный ток преобладает над влиянием анодного напряжения Ua. Поэтому незначительное изменение сеточного напряжения вызывает значительное изменение анодного тока. При достаточно большом отрицательном заряде на сетке ее электрическое поле может оказаться сильнее анод-ис ного поля. [36]
Несмотря на успешное исследование излучательной рекомбинации 280 ], действие ее слабо ( что подтверждает малую величину коэффициента поглощения, применимого к подобным переходам. Конечно, иногда не следует пренебрегать несобственными переходами типа Оже. Особенно если ловушки имеют большой отрицательный заряд. Однако преобладающим механизмом ( по крайней мере, в германии и кремнии, где он был основательно изучен), является рекомбинация с эмиссией фононов. Теория эта была разработана Лаксом [282], причем она дает долю рекомбинации достаточной величины для объяснения малых значений т, полученных при измерении. [37]
 |
Электростатический распылитель Стэджет. [38] |
Электростатическое напыление полиэтилена является сравнительно новым способом получения покрытий, однако он получил уже промышленное оформление. Сущность его заключается в том, что слой полиэтиленового порошка удерживается на поверхности изделия мощными силами электростатического притяжения в течение многих часов и таким образом процессы напыления и оплавления могут быть разделены во времени, что очень важно при обработке больших поверхностей. При напылении полиэтиленовому порошку сообщается большой отрицательный заряд от системы электродов. Для этого созданы электростатические распылители ( рис. 90) с измененной аэродинамикой, поскольку обычные распылители с движением порошка по оси сопла не обеспечивают равномерного распределения порошка по поверхности. [39]
Два атома фтора, связанные водородной связью, находятся друг от друга на расстоянии 2 55 А. Расстояние Н - F в простой молекуле HF равно 0 92 А. Фтор, имеющий из всех элементов самый большой отрицательный заряд, образует наиболее устойчивые водородные связи. Помимо фтора, устойчивые водородные связи образуют также кислород и азот. [40]
Положительные трехвалентные ионы, например La3 или Ри3, имеют относительно малую склонность к комплексообразованию, но положительные четырехвалентные ионы Ме4 и гидратированные положительные ионы шестивалентных металлов МеОг образуют устойчивые комплексы. Устойчивость комплекса зависит также от свойств комплексообразующего аниона. Прочные комплексы обычно образуются с анионами слабых кислот или же с анионами, имеющими малый атомный радиус и большой отрицательный заряд. [41]
С другой стороны, некоторые приведенные в табл. 5.3 молекулы могут оказаться и неустойчивыми. Фторат-ион РОз может быть энергетически неустойчивым, поскольку центральный атом фтора очень невелик, и три атома кислорода не могут комфортабельно расположиться вокруг него. Азотные аналоги сульфит - и сульфат-ионов, МОГ и МОГ, вероятно, не существуют потому, что это потребовало бы накопления слишком большого отрицательного заряда на молекуле с небольшим центральным атомом. [42]
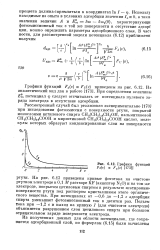 |
Графики функций Fd ( v и Fv ( v ]. [43] |
На рис. 6.13 приведены кривые фототока на чистом ртутном электроде в 0 1 М растворе KF ( акцептор N20) и на том же электроде, покрытом цетиловым спиртом в результате натирания поверхности ртути под раствором кристалликом этого органического вещества. При потенциалах от - 0 6 до - 1 2 в адсорбция спирта уменьшает фотоэмиссионный ток в десятки раз. Подъем тока при - 1 2 б и выход на кривую 1 ( для чистого электрода) объясняется разрушением слоя цетилового спирта при большом отрицательном заряде поверхности электрода. [44]
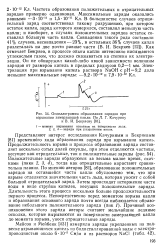 |
Осциллограмма образования зарядов при. [45] |
Страницы: 1 2 3 4