Кривое заряжение
Cтраница 3
Сравнивая кривые заряжения рис. 2 и рис. 3, можно видеть, что снятие кривых заряжения в соляной кислоте протекает при более равновесных условиях. [32]
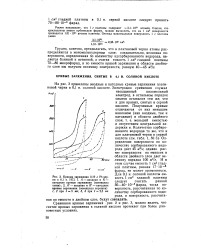
Из кривых заряжений, снятых при 15, 24 и 48 С, рассчитаны по уравнению Клаузиуса-Клапейрона дифференциальные теплоты сорбции. Полученные данные приведены на рис. 7 и 8, При заполнении, соответствующем 0 1 г-ат Н / г-ат сплава ( рис. 8, кривая /), теплота растворения водорода в сплавах незначительно падает с ростом содержания родия в сплайе; при больших заполнениях ( например, 0 3 г-ат Н / г-ат сплава) ( рис. 8, кривая 2) наблюдается более резкое падение теплоты растворения с увеличением содержания Rh в сплаве. [33]
Анализ кривых заряжения показывает, что при гальванической анодной поляризации потенциал, приобретаемый сталью, может значительно превысить критическое значение ( фп), обычно определяемое потенциостатическим методом, а сталь заметной питтинговой коррозии не подвергается. [34]
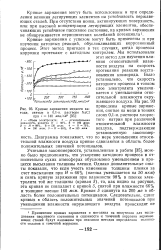 |
Кривые заряжения медного катода, снятые в 0 1 - н. растворе NaCl при i 140 мка / см2. [35] |
Применение кривых заряжения и методика их получения для исследования пассивного состояния и склонности точечной коррозии нержавеющих сталей будут изложены при описании методов определения склонности сплавов к точечной коррозии. [36]
Анализ кривых заряжения показывает, что при гальваностатической анодной поляризации потенциал, приобретаемый сталью, может значительно превысить критическое значение ( рп), обычно определяемое потенциостатическим методом, а сталь заметной питтинговои коррозии не подвергается. Активноработающие питтинги на электроде появляются лишь тогда, когда на кривой заряжения исчезают периодические колебания потенциала, что достигается при определенной плотности анодного тока. [37]
Анализ кривых заряжения и спада потенциала методом, рассмотренным выше ( раздел VI, 1), дает возможность рассчитать параметр /, основываясь на квазиравновесной трактовке. [38]
Анализ кривых заряжения, снятых после контакта родиевого и платино-рутениевого электродов с разбавленными растворами метанола, показывает равенство количеств электричестваг затрачиваемых на окисление адсорбированных при фг водорода и органического вещества. [39]
Методом кривых заряжения было установлено [12], что водород адсорбируется в заметных количествах на платине, иридии, радии, никеле и серебре. [40]
Метод кривых заряжения применяют также при исследовании адсорбции органических соединений на электродах. В этом случае наиболее целесообразно использовать метод быстрого заряжения и по количеству электричества, пошедшего на восстановление или окисление вещества, определять его адсорбцию. [41]
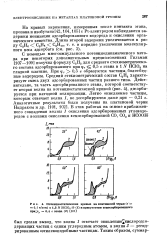 |
Потендиостатические кривые аа платиновой черви ( 0 1 в / сек в 4 3 N НС1О410 ( 1 и присутствии хеносорбировавного приг 0 4 в этана ( Я. [42] |
На кривых заряжения, измеренных после контакта этана, пропана и изобутана [42,104,105] с Pi-электрод ом наблюдаются задержки ионизации адсорбированного водорода и окисления органического вещества. [43]
Метод кривых заряжения широко применяется при изучении процессов адсорбции и строения двойного слоя на электродах из платиновых металлов. [44]
Метод кривых заряжения позволяет изучать адсорбцию и других веществ. [45]
Страницы: 1 2 3 4 5