Измерение - скорость - реакция
Cтраница 1
Измерение скоростей реакции при сочетании аминов в пределах рН 2 - б показало, что скорость возрастает до некоторого предела, соответствующего максимальной концентрации свободного амина. Таким образом, амин взаимодействует в виде основания, а не в форме соли. [1]
Измерение скоростей реакции при сочетании аминов в пределах рН 2 - 6 показало, что скорость возрастает до некоторого предела, соответствующего максимальной концентрации свободного амина. Таким образом, амин взаимодействует в виде основания, а не в форме соли. [2]
Измерение скорости реакции при сочетании аминов в пределах рН 2 - 6 показало, что скорость возрастает до некоторого предела, соответствующего максимальной концентрации свободного амина. Таким образом, амин взаимодействует в виде основания, а не в форме соли. [3]
Измерение скоростей реакций и исследование факторов, которые на них влияют, составляют важные элементы изучения как механизмов реакции, так и химической реакционной способности в целом. [4]
Измерение скорости реакции проводят амперометрически. [5]
Измерение скорости реакции в лабораторном масштабе обычно осуществляется в условиях, исключающих влияние побочных факторов. Как правило, исследования ведутся при постоянных температуре, давлении и интенсивном перемешивании. Полученные таким образом кинетические данные очень полезны для изучения механизма реакции, но, как правило, не касаются количественной оценки скорости процесса. [6]
Измерения скоростей реакций были проведены на плоской грани монокристалла меди в присутствии указанных выше веществ при 350 и смеси газа, состоящей из 95 % водорода и 5 % кислорода [28]; при этом как структура поверхности, так и каталитическая активность различных граней изменялись под влиянием данных веществ. На рис. 11 представлены микрофотографии таких поверхностей после проведения на них реакции в течение 20 час. [7]
Измерение скорости реакции основано на определении концентрации одного из реагирующих веществ через различные промежутки времени с момента начала реакции. [8]
Измерение скорости реакции, основано на определении концентрации одного из реагирующих веществ через различные промежутки времени с момента начала реакции. [9]
Измерение скорости реакции в открытых системах можно проводить стат-методом, который предполагает введение реагентов со скоростью, равной скорости их расходования в реакции, так что концентрация индикаторного вещества остается постоянной. Скорость введения реагента регулируется автоматически. [10]
Измерение скоростей реакции при сочетании аминов в пределах рН 2 - 6 показало, что скорость возрастает до некоторого предела, соответствующего максимальной концентрации свободного амина. Таким образом, амин взаимодействует в виде основания, а не в форме соли. [11]
Измерения скорости реакции на контактах с различной удельной поверхностью и различной степенью науглероженности проводили в одинаковых условиях для получения сравниваемых результатов, а именно при температуре 1200 и концентрации водорода 80 % в исходной смеси метан - водород. Эти условия выбраны, исходя из того, что при них практически не протекает объемный процесс разложения метана, искажающий результаты. Кроме того, эти условия соответствуют реальным условиям протекания изучаемого процесса. [12]
Измерение скорости реакции в диффузионной области ничего не может сказать нам об истинной кинетике реакции и ее химическом механизме. Но зато измерение скорости реакции в диффузионной области может служить методом исследования диффузионных процессов, в частности конвективной диффузии. [13]
Измерение скорости реакции основано на определении концентрации одного из реагирующих веществ через различные промежутки времени от начала реакции. [14]
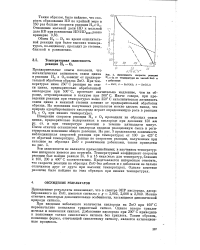 |
Зависимость скорости реакция Н2 с Оа от температуры на чистой ZnO и с добавками 1 - ZnO. 2 - ZnO ( Al. 3 - ZnO ( Li. [15] |
Страницы: 1 2 3 4