Измерение - энтальпие - сгорание
Cтраница 2
Одним из наиболее важных методов определения энтальпий образования органических соединений является измерение энтальпий сгорания их в кислороде. Широкое использование различных вариантов этого метода обусловлено тем, что для очень большого числа органических соединений реакция сгорания в кислороде - процесс, удобный для калориметрического измерения. [16]
Основной методикой, используемой при термохимическом изучении органических веществ, является измерение энтальпий сгорания их в кислороде. Этой области термохимии в течение длительного ряда лет посвящены усилия многих термохимиков мира. В ней накоплен очень богатый экспериментальный материал и многие экспериментальные приемы детально разработаны. [17]
Одним из наиболее важных методов определения энтальпий образования органических соединений является измерение энтальпий сгорания их в кислороде. Широкое использование различных вариантов этого метода обусловлено тем, что для очень большого числа органических соединений реакция сгорания в кислороде - процесс, удобный для калориметрического измерения. [18]
Батареи термопар редко используют для измерения температуры калориметров, предназначенных для измерения энтальпий сгорания. Основным затруднением является при этом необходимость поддержания температуры побочных спаев с очень высокой точностью. Однако в работе Магнуса и Беккера [9] ( см. выше) говорится о том, что высокая точность результатов была достигнута при измерении температуры калориметра батареей термопар. [19]
Измерение энтальпий хлорирования веществ проводят в калориметрической практике значительно реже, чем измерение энтальпий сгорания в кислороде. Вызывается это в основном меньшей по сравнению с кислородом доступностью чистого хлора и тем, что работа с этим реагентом связана со значительно большими трудностями в отношении защиты деталей аппаратуры и коммуникаций от коррозии, чем работа с кислородом. [20]
Измерение энтальпий фторирования твердых веществ связано со значительно большими трудностями, чем измерение энтальпий сгорания в кислороде и энтальпий хлорирования. Определяется это очень высокой реакционной способностью фтора. [21]
При наличии достаточно точных электроизмерительных приборов и достаточно стабильных источников тока тепловое значение калориметра, предназначенного для измерения энтальпий сгорания, может быть определено методом градуировки калориметра электрическим током ( рекомендации об использовании этого метода см. в I, стр. [22]
Остальные детали калориметрических установок ( калориметрический сосуд, оболочка, измерители температуры и др.) могут быть такими же, что и при измерении энтальпий сгорания органических веществ. [24]
Кроме того, целесообразно вначале ограничить описание случаями, когда подлежащие сожжению вещества при комнатных температурах являются твердыми или жидкими, так как методика измерения энтальпий сгорания газов и паров существенно иная; она будет описана отдельно ( см. гл. [25]
Реакции между твердым ( или жидким) и газообразным веществами, энтальпии которых приходится измерять, в зависимости от характера газообразного реагента можно разделить на несколько подгрупп - реакции окисления кислородом, фторирования, хлорирования, гидрирования и др. Наибольшее число термохимических работ по изучению этих реакций посвящено измерению энтальпий сгорания веществ в кислороде. В данном параграфе дается представление о термохимическом исследовании указанных реакций и о состоянии данной области термохимии в настоящее время. [26]
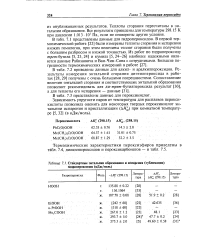 |
Стандартные энтальпии образования и испарения ( сублимации гидропероксидов ( кДж / моль. [27] |
В табл. 7.2 приведены данные для алкил - и аралкилпероксидов. Результаты измерения энтальпий сгорания диэтилпероксида в работах [28, 29] получены с очень большими погрешностями. [28]
Поэтому в настоящее время к электрической градуировке калориметров прибегают редко, главным образом в метрологических учреждениях, занятых приготовлением и исследованием эталонных веществ для калориметрии. В подавляющем большинстве работ по измерению энтальпий сгорания определение теплового значения калориметра проводится с использованием препаратов эталонной бензойной кислоты. [29]
Объясняется это прежде всего тем, что подобрать удовлетворительные условия сожжения большей части металлов трудно, а некоторых - просто невозможно. Так, например, практически нельзя рассчитывать на измерение энтальпий сгорания благородных металлов - платины, золота, серебра, паладия, родия и др. Среди металлов, для которых очень трудно подобрать удовлетворительные условия сожжения, можно назвать медь, олово и некоторые др. Термохимические работы по измерению энтальпий сгорания всех перечисленных металлов отсутствуют. Также до сих пор не измерены ( вследствие крайней малодоступности препаратов) энтальпии сгорания ряда радиоактивных элементов: франция, прометия, полония, протактиния и всех актинидов, начиная с кюрия. [30]
Страницы: 1 2 3