Анион - бром
Cтраница 3
Для анодного активирования ниобия и тантала и поддержания активированного состояния необходима достаточно высокая концентрация КВг. Предполагается, что при определенных условиях анионы брома могут входить в окисную пленку, образуя с металлом промежуточное соединение. Далее М2О5 образуется не в результате непосредственного взаимодействия металла и кислорода ( как при оксидировании металлов), а в результате гидролиза промежуточного соединения металла с бромом и представляет собой не сплошную защитную пленку, а отдельные частицы, спадающие с электрода и не препятствующие растворению анода. [31]
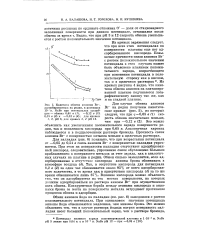 |
Кинетика обмена анионов Br -, Для случая обмена анионов. [32] |
При одинаковом значении потенциала анионы йода обмениваются медленнее, чем анионы брома. [33]
С - Н - связи включает как изгиб, так и растяжение связи, можно ожидать, что будет проявляться лишь небольшой кинетический изотопный эффект ( см. книгу Белла в списке общей литературы, стр. Кинетика окисления молекулярным бромом усложняется тем, что по мере образования анионы брома выводят из реакции эквивалент брома в виде неактивного комплексного аниона Br - f, но эту трудность можно обойти, используя в качестве окислителя бромат. К тому же бром быстро вступает в реакцию замещения с образующимися альдегидами или кетовами Показано, что в кислом растворе начальная скорость окисления этанола не зависит ни от кислотности, ни от концентрации иона брома, а поэтому альтернативный механизм окисления через обратимое окисление до эфира гипобромита может быть отвергнут. [34]
С) был выделен с выходом 12 % и охарактеризован по УФ-спектру, который свидетельствует об отсутствии сопряжения, и по превращению в к-тетрадекан при исчерпывающем гидрировании. Во второй стадии реакции хлористая медь ускоряет превращение бромистого аллила вследствие координации катиона меди с отщепляющимся анионом брома ( ср. [35]
С) был выделен с выходом 12 % и охарактеризован по УФ-спектру, который свидетельствует об отсутствии сопряжения, и по превращению в и-тетрадекан при исчерпывающем гидрировании. Во второй стадии реакции хлористая медь ускоряет превращение бромистого аллила вследствие координации катиона меди с отщепляющимся анионом брома ( ср. [36]
Кабанов и Лейкис выявили ускоряющее влияние адсорбции иона ОН - на кинетику растворения железа, а работы Колотыркина с сотрудниками показали, что первичный акт растворения большого числа металлов протекает через образование комплексов с участием адсорбированных анионов. Иофа, адсорбция органических оснований и их ингибирующее действие на кислотную коррозию железа и кобальта резко возрастают в присутствии анионов брома и йода, сообщающих поверхности отрицательный заряд. [37]
Различной электроотрицательностью и сродством к электрону объясняется вытеснение одних галогенов другими из их соединений. Так, у фтора наибольшая электроотрицательность и сродство к электрону, он может отнимать электроны от любых галогенов; хлор отнимает электроны только от анионов брома и иода, а бром только от анионов иода. [38]
Начальным актом этой реакции является атака бедным электронами атомом брома, как это было показано на примерах присоединения к алкенам, а в согласии с П 8 она должна происходить преимущественно в конце цепи. При этом образуется ион, могущий, как показано на схеме, подвергаться таутомерному превращению, в результате которого в молекуле образуются две возможные точки для присоединения аниона брома. [39]
Галогены могут присоединяться по радикальному ( инициатором является свет) и по ионному механизму. При ионном галогениро-вании взаимодействие я-электронов этилена с электрофильной молекулой брома приводит к образованию я-комплекса, который превращается далее в результате образования связи между положительно заряженными атомами брома и атомом углерода в карбокатион, стабилизирующийся взаимодействием с анионом брома. [40]
Таким образом, нуклеофильная активность этиленовой двойной 1 связи проявляется предпочтительно по сравнению с электрофильной активностью, которая проявляется лишь во второй стадии. То, что подобные отношения действительно имеют место, можно доказать кинетическими исследованиями, а Также тем фактом, что реакция ускоряется при повышении концентрации ионов водорода. Повышение же концентрации анионов брома не влияет на скорость реакции. [41]
Стереохимическое направление присоединения брома к двойной связи холестерина служит для иллюстрации ряда стереоэлектронных принципов, изложенных выше. Во второй стадии трехчленный цикл раскрывается при приближении аниона брома к С-6 с р-стороны. Только такой путь обусловливает полное транс ( диакси-альное) раскрытие цикла. Начальный продукт термодинамически неустойчив по сравнению с его экваториально-экваториальным изомером, поскольку объемистые атомы брома занимают сравнительно пространственно затрудненные аксиальные положения в 5а, бр-изомере. Если это вещество оставить в хлороформе, то первоначальный диаксиальный изомер претерпевает внутримолекулярную перегруппировку в устойчивый 5) 3, ба-изомер. [42]
Стереохимическое направление присоединения брома к двойной связи холестерина служит для иллюстрации ряда стереоэлектронных принципов, изложенных выше. Во второй стадии трехчленный цикл раскрывается при приближении аниона брома к С-6 с ( З - стороны. Только такой путь обусловливает полное транс ( диакси-альное) раскрытие цикла. Начальный продукт термодинамически неустойчив по сравнению с его экваториально-экваториальным изомером, поскольку объемистые атомы брома занимают сравнительно пространственно затрудненные аксиальные положения в 5а, б - изомере. Если это вещество оставить в хлороформе, то первоначальный диаксиальный изомер претерпевает внутримолекулярную перегруппировку в устойчивый 5 3, Оа-изомер. [43]
Активация малоактивных металлов, например титана, ниобия и сплавов на их основе, связанная с пробоем образующихся на их поверхности пассивных пленок, происходит при гораздо более высоких анодных потенциалах - потенциалах пробоя и сопровождается значительным ростом плотности тока и скорости растворения. Величина потенциала пробоя определяется в основном стойкостью пассивирующих пленок обрабатываемого металла и активирующими свойствами электролита, зависящими от анионного состава, рН и температуры электролита. Применительно к титану и сплавам на его основе наибольшей способностью к пробою пассивных пленок обладают анионы брома. [44]
Примером такой реакции, сопровождающейся перегруппировкой углеродного скелета, служит реакция гетеролиза неопентилбромида. Несмотря на то что этот бромид - первичный алкилгалогенид, он практически не способен к реакциям нуклеофильного замещения по механизму 5N2 из-за пространственных затруднений, создаваемых разветвленным трег-бутиль-ным радикалом при подходе нуклеофильного реагента. Однако его можно заставить реагировать по механизму 5N1 в присутствии водных растворов солей серебра, так как ион серебра вырывает из молекулы алкилгалогенида анион брома, образуя бромид серебра. [45]
Страницы: 1 2 3 4