Анион - галоген
Cтраница 2
На следующей стадат он присоединяет анион галогена по положительно заряженному углероду. [16]
Из уравнений следует, что анионы галогенов принимают непосредственное участие в электродной реакции или в предшествующих ей химических стадиях. [17]
При присоединении галогенов в присутствии анионов другого галогена образуются аддукты, содержащие оба галогена. Совершенно аналогично вода и спирты приводят к галогенгидри-нам или галогенэфирам. [18]
Хром в водных растворах, содержащих анионы галогенов, не склонен к ПК - Только низкое содержание воды в электролите создает условия для питтингообразования. [19]
Образование этих соединений подтверждает общеизвестную аналогию свойств анионов галогенов и циановой и тиоциановой кислот. [20]
Реакции отщепления, в которых уходящие группы - анион галогена и протон - отщепляются от соседних атомов углерода с образованием тг-свя-зи между ними, называют - элиминированием. [21]
 |
Амфотерные гидроксиды. [22] |
Эффективный способ получения простых катионов в комбинации с анионом галогена заключается в прямой реакции металла с галогеном. Большинство металлов легко окисляются по крайней мере наиболее активными галогенами, и образующиеся галогенидные соли, за исключением содержащих катионы Ag, Pb2 и Hg2, растворимы в воде, откуда их можно извлечь и получить в очищенном виде. О легкости, с которой протекают эти реакции, можно судить по данным об энергиях образования галогенидов щелочных металлов, приведенным в табл. 19.5. Соединение щелочных металлов с фтором происходит со взрывом, а их реакции с хлором и бромом протекают самопроизвольно. [23]
Анионами, образующими с катионами ионные пары, были изо-структурные анионы галогенов С1 -, Вг - и J и близкие к ним по размерам NOa, SCN - nC104, а также двухзарядный аннон SOf Для экстракции были избраны два растворителя, инертный в отношении диссоциации красителя хлороформ ( диэлектрическая проницаемость равна 4 8) и диссоциирующий. [24]
Можно полагать, что для таких простых ионов ( анионов галогенов) образование ионных ассоциаций электростатической природы будет происходить тем реже, чем больше размер иона. [25]
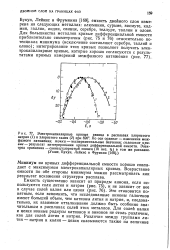
На рис. 2 показана зависимость теплоты гидратации солей от аниона галогена и от катиона щелочного металла. [26]
Можно полагать, что для таких простых ионов ( анионов галогенов) образование ионных ассоциаций электростатической природы будет происходить тем реже, чем больше размер иона. [27]
На рис. 2 показана зависимость теплоты гидратации солей от аниона галогена и от катиона щелочного металла. [28]
Реакции заключаются в ацилировании гидроксиль-ной группы с последующим замещением анионом галогена по механизму ЗыАг или при термическом разложении эфира. Реакции первого типа реализуются в соединениях, где гидроксильная группа находится под сильным электроакцепторным влиянием: в ди - и тринитрофенолах и в гидроксигетероциклах. Термическое разложение эфиров позволяет замещать гидроксильную группу в неактивированных соединениях. [29]
Страницы: 1 2 3 4