Анион - галоген
Cтраница 3
Это становится по - нятным, если вспомнить, что исследованные анионы галогенов имеют больший объем, чем катионы лития и натрия, и, следова тельно, их взаимное отталкивание должно быть особенно значительным в расплавах солей этих металлов. Для солей калия и цезия ионные радиусы катионов и анионов не столь различны, как для солей лития и натрия. [31]
Во всех приведенных выше случаях источниками анионов, конкурирующих с анионами галогена в процессе присоединения к олефину, служили другие вещества, добавленные в реакционную смесь. Известны, однако, случаи, когда таким - конкурирующим анионом является неуклеофильная группа самого олефина. [32]
Во всех приведенных выше случаях источниками анионов, конкурирующих с анионами галогенов в процессе присоединения к олефину, служили другие вещества, добавленные в реакционную смесь. Известны, однако, случаи, когда таким конкурирующим анионом является нуклеофильная группа самого олефина. [33]
Естественно, что порядки связей с уходящим атомом галогена и анионом галогена, выступающим в роли нуклеофнла, равны вследствие симметрии системы. В случае бензилгалогенидов рыхлость-сжатость переходного состояния меняется в пределах одной реакционной серии, поэтому реакция ускоряется как электроно-акцепторными, так и электронодонорными заместителями. [34]
В качестве уходящей группы при нуклеофильном замещении не обязательно должен выступать анион галогена. Некоторые другие электроотрицательные группы, которые при гетеро-литическом расщеплении связи с углеродом ( разд. Пример реакции подобного типа был приведен ранее при рассмотрении метода получения алкилгалогенидов из спиртов. [35]
По мнению авторов работы [27], первоначально образуется неустойчивый анион-радикал, отщепляющий анион галогена. [36]
На первой стадии происходит медленная ионизация алкил-галогенида с образованием карбокатиона и аниона галогена. Затем следует очень быстрое взаимодействие нуклеофила с карбокатионом, приводящее к продукту нуклеофильного замещения. [37]
Бергельсон и Шемякин [86] предположили, что в результате комплексообразов ания аниона галогена с фосфониевой группой - молекулы нестабильного илида может понизиться реакционная способность последнего. Если в комплексообразовании участвует фосфониевая группа, то учет электронных факторов подсказывает, что илид должен стать более нуклеофильным. Такое влияние комплексообразования может быть компенсировано стерическими факторами, препятствующими атаке карбаниона на карбонильную группу. [38]
Для оксокатионов элементов шестой группы характерны комплексы MeOX4Y, где Х - - анион галогена или другой кислоты. [39]
Большинство неорганических и органических галогенидов дает при диссоциации или при реакциях с нуклеофильными группами анионы галогенов, в которых галоген сохраняет также связывающие электроны бывшей ковалентной связи. Вместе с тем есть много соединений галогенов, типичным представителем которых является хлорноватистая кислота НОС1, являющихся окислителями, способными выделять иод из растворов йодистого калия. [40]
 |
Три механизма окислительного присоединения к плоской молекуле. [41] |
Вторым типом экспериментов с захватом является введение большого избытка некоторого аниона, отличного от аниона галогена алкилгалогенида. [42]
Если цикл активирован, р-ция может протекать по ионному механизму, к-рый включает стадию присоединения аниона галогена к промежуточно образующемуся в процессе электроф. [43]
Образовавшиеся сложные эфиры подвергаются ионизации с удалением аниона галоида, вслед за которой происходит замещение анионом галогена по механизму нуклеофильного замещения. Реакции этого типа реализуются в соединениях, где гидроксильная группа находится под сильным электроноакцепторным влиянием. В данном случае такое влияние оказывают атомы азота триазинового кольца, которые, являясь по своей природе электроотрицательными элементами, смещают электронную плотность в свою сторону, что приводит к обеднению кольца электронами. [44]
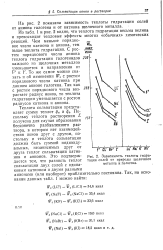 |
Зависимость теплоты гидратации солей от природы щелочного металла и галогена. [45] |
Страницы: 1 2 3 4