Крупный анион
Cтраница 2
Перечисленные и многие другие крупные катионы аналогичного состава способны сочетаться с крупными анионами, образуя экстрагирующиеся ионные ассоциагы. К таким крупным анионам относятся, например, следующие. [16]
 |
Свойства некоторых карбонилгидридов. [17] |
Как правило, такие ионы известны только в виде солей со сравнительно крупным анионом. [18]
Вначале полагали, что низкая энергия кристаллической решетки продукта с крупным катионом и крупным анионом настолько мала, что соединение не кристаллизуется даже при комнатной температуре. Однако такие соединения, как тетрафенилбо-рат ( Ш) триэтиламмония и дибромокупрат ( 1) триэтиламмония, оба твердые, хотя содержат еще более крупные анионы. [19]
Энергия гидратации крупных ионов невелика, поэтому такие катионы или катионные комплексы осаждаются в присутствии крупных анионов или анионных комплексов. Растворимость комплексных солей определяется совокупностью следующих факторов: отношение радиусов ионов, составляющих данную соль, должно приближаться к определенному значению ( 0 7 - 1 2); увеличение заряда комплексного иона способствует уменьшению растворимости. [20]
К ионным ассоциатам относят соединения, со-стоящие из крупных катионов и, как правило, крупных анионов с малым зарядом. В водных растворах они распадаются на ионы, в органической фазе - присутствуют в неионизированном состоянии. [21]
Учитывая, что калий, являясь крупным катионом, должен давать прочное малодиссоциированное соединение с крупным анионом [7] кремнефтористоводородной кислоты, в 1959 году одним из нас было успешно выполнено концентрирование примеси 1 10 - 4 % кремния в плавиковой кислоте выпариванием 20 мл этой кислоты с добавкой 10 мг хлористого калия и 0 05 г угля. [22]
В работе Кришнана и Фридмана [20] были измерены энтальпии растворения в диметилформамиде ряда солей с крупными анионами и катионами. [23]
 |
Диаграмма плавкости системы KCl-NaCl - Na3A. F a. [24] |
Понижение электропроводимости флюса может также достигаться введением криолита иди других комплексных солей, так как подвижность крупных анионов A1F; в расплаве почти на два порядка ниже, чем катионов натрия. [25]
 |
Влияние пятиоки-си фосфора на поверхност-ное натяжение расплава СаО - Р2О5, согласно. А - зависимость по данным Брэдбери. [26] |
При повышении температуры происходит диссоциация комплексов средней сложности и образование как более простых, так и более крупных анионов. [27]
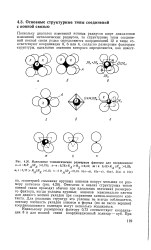 |
Идеальные топологические размерные факторы для координации. [28] |
Описание и анализ структурных типов ионной связи проводят обычно при идеальных значениях размерного фактора, когда укладка крупных анионов максимально плотна для данного мотива укладки при сохранении катион-анионного контакта. Для реальных структур это условие не всегда соблюдается, поэтому плотность укладки анионов и форма ( но не число вершин) координационного полиэдра могут несколько искажаться. [29]
При введении в электролит конго красного или п-бензолсульфо-азо-нафтилам на, применяемых в виде натриевых солей сульфокислот, в растворе образуются крупные анионы этих соединений, которые вступают в реакцию с комплексными катионами Cu ( CSN2H4) 4, образуя нейтральные молекулы. Это предотвращает их разряд и включение в осадок и, таким образом, устраняет хрупкость. По-видимому, на адсорбцию тиомочевины эти добавки не влияют, так как блеск медных осадков не ухудшается. [30]
Страницы: 1 2 3 4 5