Термодинамическое измерение
Cтраница 2
Многие из этих веществ структурно родственны декалину, транс-форма которого является более устойчивой, что установлено термодинамическими измерениями и опытами по изомеризации. [16]
Многие из этих веществ структурно родственны декалину, транс-форыа которого является более устойчивой, что установлено термодинамическими измерениями и опытами по изомеризации. [17]
Второе начало термодинамики согласно (1.56), (1.57) позволяет вычислять изменения энтропии системы при конечных равновесных изменениях ее состояния на основании результатов калориметрических и термодинамических измерений. [18]
При сравнении изостерических или калориметрических теплот с энергиями активации десорбции подразумевается, что изучаемый кинетический процесс имеет решающее значение и при установлении распределения, преобладающего в термодинамических измерениях. [19]
Поскольку энтальпийная функция дает вклад в изменение энергии Гиббса ДОАЯ-Т AS, можно ожидать, что именно для эндотермического процесса наиболее вероятна ограниченная растворимость; это в действительности подтверждается термодинамическими измерениями. Однако на молекулярном уровне эндотермический ход процесса растворения обусловлен тем, что однородные частицы в чистых жидкостях притягивают друг друга в смеси в среднем сильнее по сравнению с разнородными. Следовательно, для разделения однородных частиц в систему необходимо ввести больше энергии, чем выделится при сближении разнородных частиц в процессе смешения. [20]
 |
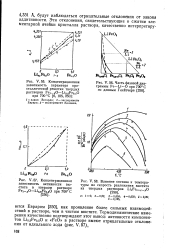
Схема, иллюстрлрующая связь между величинами дД (, дф в др.. [21] |
Как показал Гуггенгейм и как вытекает, в сущности, из цитированной работы Бренстеда, в рамках термодинамики соотношение (1.4) следует рассматривать как чисто формальное, поскольку на основе каких-либо термодинамических измерений невозможно приписать величинам ч и р определенные значения. Рассмотрим, например, некоторую проводящую конденсированную фазу А ( рис. 1.1 а), состоящую из внутренней однородной части /, поверхностного двойного слоя 2 и избыточного заряда 3, который на рисунке показан положительным. [22]
На фазовой диаграмме ксеноновой плазмы, представленной в качестве примера на рис. 1.5, сплошными линиями указаны области одно - и двукратной ионизации, а также отмечены точки, для которых выполнены термодинамические измерения. Из-за высоких температур и особенностей электронных оболочек в такой плазме отсутствуют молекулярные и кластерные образования, а из-за малого количества нейтральных частиц превалирующим типом межчастичного взаимодействия является чисто кулоновское. [23]
Поскольку энтальпийная функция дает вклад в изменение свободной энергии, ДО АЯ-Г AS, можно ожидать, что именно в случае эндотермического процесса наиболее вероятна ограниченная растворимость; это в действительности подтверждается термодинамическими измерениями. Однако па молекулярном уровне причина эндотермических процессов должна заключаться в том, что одинаковые частицы в чистых жидкостях притягивают друг друга в среднем сильнее, чем неодинаковые частицы в смеси. Следовательно, для разделения одинаковых частиц в систему необходимо ввести больше энергии, чем выделится при сближении разнородных частиц в процессе смешивания. [24]
Поскольку энтальпийная функция дает вклад в изменение свободной энергии, ЛО ДЯ-Г AS, можно ожидать, что именно в случае эндотермического процесса наиболее вероятна ограниченная растворимость; это в действительности подтверждается термодинамическими измерениями. Однако на молекулярном уровне причина эндотермических процессов должна заключаться в том, что одинаковые частицы в чистых жидкостях притягивают друг друга в среднем сильнее, чем неодинаковые частицы в смеси. Следовательно, для разделения одинаковых частиц в систему необходимо ввести больше энергии, чем выделится при сближении разнородных частиц в процессе смешивания. [25]
С целью поиска корректных подходов к конформационному анализу 1 3-диоксанов в рамках программного обеспечения HyperChem исследована применимость эмпирического ( ММ), а также полуэмпирических методов ( MNDO, AMI и РМЗ) к расчету оптимальной геометрии и теплот образования молекул 1 3-диоксанов I-V в сравнении с результатами рентгеноструктурных и термодинамических измерений. [26]
Именно последние представляют интерес в контексте данной книги. Термодинамические измерения позволяют количественно изучать сольватацию в - различных растворителях и непосредственно сравнивать в этом отношении растворители путем использования функций переноса. Вместе с тем существуют значительные трудности применения термодинамики процессов сольватации к реальным системам с химическими реакциями. Этот вопрос кратко рассматривается в следующем разделе наряду с основными расчетными формулами. [27]
Термодинамические измерения качественно подтверждают этот вывод: активности компонентов Lio. [29]
Вся сумма имеющихся в настоящее время данных подтверждает мнение о том, что термодинамические константы, описывающие связывание железа с трансферрином, внутренне идентичны. Физиологическое исследование Шэйда не содержало термодинамических измерений и поэтому не противоречит предшествующим результатам. Количественных данных о связывании железа с лактоферрином в настоящее время не имеется. [30]
Страницы: 1 2 3 4