Термохимическое измерение
Cтраница 3
Теоретические представления о термохимическом измерении сродства получают большое распространение в 70 - 80 - х годах XIX в. Но термохимики не могли объяснить причины подвижных химических равновесий; принцип наибольшей работы, как подчеркивал Бертло, есть принцип статический, он не допускал существования подвижных равновесий. [31]
 |
Сравнение жадности кислот. [32] |
Томсен получал эти коэфициенты из термохимических измерений, Оствальд - из сравнения удельных объемов растворов реагирующих веществ и удельного объема реакционной смеси. [33]
Действительно, как известно из термохимических измерений Томсена, теплота нейтрализации разбавленных растворов всех сильных кислот и оснований одинакова, так как представляет собой тепловой эффект образования воды из иона водорода и гидроксилз. [34]
 |
Молярная энтропия некоторых веществ при 25 С и 1 атм. [35] |
Вычисление изменений энтропии основывается на результатах термохимических измерений, но определение абсолютных значений энтропии требует, кроме того, установления условной точки ее отсчета. Принято, что энтропия совершенного кристалла при температуре абсолютного нуля равна нулю ( в такой системе полностью устраняется всякая неупорядоченность) и что энтропия всех веществ при приближении к О К стремится к нулю. [36]
Однако метод определения термодинамических параметров углеводородов путем непосредственных термохимических измерений весьма трудоемок, сложен и требует наличия веществ очень высокой степени чистоты. Фактически даже в фундаментальных работах Россини и его школы непосредственно экспериментальным измерениям подвергались лишь некоторые ключевые углеводороды. Термодинамические же параметры остальных углеводородов рассчитывались на основании методов подобия и структурных групп. Поэтому наряду с термохимическими методами оценки термодинамических параметров различных углеводородов параллельно развивались исследования по экспериментальной оценке их относительной термодинамической устойчивости путем изучения состава равновесных смесей изомеров. [37]
В этом случае удается подтвердить вышесказанное непосредственнными термохимическими измерениями. Так, например, известно [51], что первые порции кислорода адсорбируются углем с выделением очень большого количества тепла, приблизительно 220 ккал / моль. Дифференциальная теплота адсорбции последующих порций кислорода быстро уменьшается. [38]
Совпадение энергий диссоциации связей, полученных из термохимических измерений и из кинетических исследований, показывает, что введение нитрогруппы к одному углеродному атому правильно учтено в термохимическом расчете. Эффективное влияние нитрогрупп друг на друга близко к истинному ослаблению связей С-N в молекуле при последовательном введении нитрогруппы к одному атому углерода. Этот вывод можно использовать при расчете энергий диссоциации С-N - связи в 1 1-динитроалка-нах, которая для первых членов ряда будет приблизительно на 6 4 ккал / моль меньше, чем энергия связи С-N в соответствующем мононитросоединении, а также рассчитать энтальпии образования радикалов. [39]
Основной величиной, от которой, зависит точность термохимических измерений, является изменение температуры калориметра. Поэтому определение этой величины должно быть произведено с максимальной точностью. Если учесть, что температура обычно изменяется максимально в пределах 2 - 3, то, чтобы получить результат с точностью до одного процента, измерение температуры должно производиться с точностью до нескольких тысячных градуса. Обычные лабораторные термометры с ценой деления 0 1 для этой цели не годятся. Этому условию удовлетворяет дифференциальный термометр Бекмана, шкала которого длиной 25 - 30 см разделена на 5 - 6, а каждый градус - на десятые и сотые доли. При помощи лупы можно приблизительно измерить тысячные доли градуса. Термометр Бекмана отличается от обычных лабораторных термометров наличием дополнительного резервуара для ртути в верхней его части, который позволяет изменять количество ртути в его нижней части и таким образом приспособить термометр для работы в заданном интервале температур. [40]
Расчет теплоты образования трифторида брома, основанный на прямых термохимических измерениях, провел Стейн [41], измерив теплоту реакции фтора с бромом при 25 и 105 С. Обе величины несколько отличаются от приведенных выше, но они, вероятно, более точны. [41]
Последовательность акцепторных свойств ВВг3 ВС13 BF3 наблюдается не только по термохимическим измерениям, но и при исследовании других параметров и, по-видимому, связана не только с различиями в энергии перестройки. [42]
Для этого часто необходимо проведение большой химико-аналитической работы параллельно с термохимическими измерениями. [43]
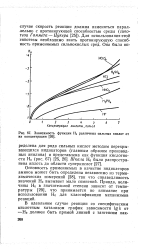 |
Зависимость функции Н0 различных сильных кислот от их концентрации. [44] |
Основность применяемых в качестве индикаторов аминов может быть определена независимо из термохимических измерений [28], так что справедливость значений Но вызывает мало сомнений. Правда, величины Но в значительной степени зависят от температуры [29], что принимается во внимание при использовании Но для классификации механизмов реакций. [45]
Страницы: 1 2 3 4