Электрохимическое измерение
Cтраница 2
 |
Установка для платинирования электродов.| Ртутный капельный электрод. [16] |
При электрохимических измерениях часто пользуются также гладкими платиновыми и платинированными электродами. [17]
В электрохимических измерениях применяют также ртутноокисный и ртутносульфатный электроды. [18]
Как показали электрохимические измерения, при такой обработке катализатора образуется прочное поверхностное кислородное соединение. Это поверхностное соединение может быть дегидрирующим катализатором, отрывая водород от молекул спирта, но оно неактивно в каталитической реакции окисления спирта. [19]
Использованные для электрохимических измерений образцы имели форму лопаток. [20]
Современная техника электрохимических измерений доведена до такого совершенства, что гальванические элементы можно по справедливости отнести к числу очень немногих систем, доступных экспериментальному исследованию в условиях полной обратимости происходящих в них процессов. [21]
Полученные результаты электрохимических измерений находятся в соответствии с данными коррозионных испытаний: после выдержки в растворе хлорида натрия шов сварных соединений, выполненных электродами МР-3 и АНО-4, подвергался коррозии менее интенсивно, чем основной металл, тогда как шов сварных соединений, выполненных электродами УОНИ 13 / 45 и АЙО-7 ч наоборот, подвергался более интенсивной коррозии по сравнению с основным металлом. [22]
В практике электрохимических измерений получили распространение электроды второго рода типа Ме / МеА / А -, где А - означает анион, находящийся в избытке легко растворимой соли КА, NaA или самой кислоты НА. [23]
Электроды для электрохимических измерений существуют нескольких типов: - стеклянные, хингидронные, сурьмяные, каломельные, хлорсеребряные и др. Каломельные и хлорсеребря-ные рассмотрены в разд. [24]
Современная техника электрохимических измерений доведена до такого совершенства, что гальванические элементы можно по справедливости отнести к числу очень немногих систем, доступных экспериментальному исследованию в условиях полной обратимости происходящих в них процессов. [25]
При проведении электрохимических измерений возникает необходимость изготовления микроэлектродов, размеры которых лимитируются величиной ячейки и заданной плотностью тока. В ряде случаев изготовление микроэлектродов сопряжено с трудностями. Образец нужного диаметра получают волочением предварительно прокатанной проволоки. Известно, например, что такие важные электрохимические параметры, как ток обмена, емкость двойного слоя и др. зависят от способа изготовления и предшествующей обработки металлического электрода. [26]
При проведении электрохимических измерений предъявляют высокие требования к чистоте растворов и поверхности электродов, в особенности от всякого рода примесей органических соединений. [27]
Поскольку большинство электрохимических измерений проводится на инертных или ртутных электродах, анодное растворение электрода в качестве причины предельного потенциала в положительной области стабильности электролита сводится в основном к растворению ртути. Анодно ртуть растворяется легко. [28]
В практике лабораторных электрохимических измерений электрохимические кулонометры служат для определения выхода по току и для других целей. [29]
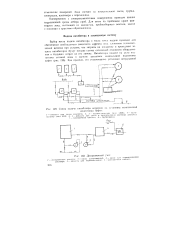 |
Схема подачи ингибитора коррозии на установке комплексной. [30] |
Страницы: 1 2 3 4