Изобара - адсорбция
Cтраница 1
Изобары адсорбции были получены при использовании обычного высоковакуумного аппарата с кварцевыми пружинными весами, применяемого для изучения адсорбции пароп пористыми телами. [1]
 |
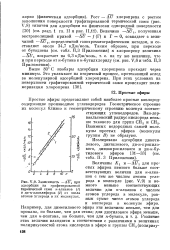
Кривые Аррениуса для низкотемпературных образцов чистой и промотированной окиси цинка при постоянной начальной скорости. [2] |
Изобары адсорбции, относящиеся к чистой окиси цинка, имеют два максимума, которые сдвигаются с изменением температуры и увеличиваются для промотированных литием образцов, но исчезают для окиси цинка, промотированной галлием. Промотирование, следовательно, изменяет неоднородность поверхности окиси цинка по отношению к водороду. [3]
Изобары адсорбции СОа из воздуха, насыщенного водяными парами при 20 0; 7 0 и 2 5 МПа, можно аппроксимировать прямыми линиями, имеющими тот же наклон, что и линия зависимости Один - от Т для осушенного воздуха, но расположенными ступенчато ниже ее в зависимости от величины рабочего давления. [4]
Изобара адсорбции газа, который может адсорбироваться на одном и том же адсорбенте как физически, так и химически, характеризуется двумя участками, вдоль которых адсорбция уменьшается с ростом температуры: один из них соответствует физической, другой - химической адсорбции. Некоторые изобары имеют три нисходящих участка, один из которых соответствует физической адсорбции, а наличие двух других свидетельствует о существовании различных типов активированной адсорбции. [5]
Изобара адсорбции газа, который может адсорбироваться на одном и том же адсорбенте как физически, так и химически, характеризуется двумя участками, вдоль которых адсорбция уменьшается с ростом температуры: один из них соответствует физической, другой - химической адсорбции. Некоторые изобары имеют три нисходящих участка, один из которых соответствует физической адсорбции, а наличие двух других свидетельствует о существовании различных типов активированной адсорбции. [6]
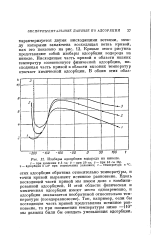
Изобара адсорбции кислорода на окиси цинка, приведенная на рис. 4, показывает, что адсорбционное равновесие достигается при температурах несколько выше 450 С. Рассмотрим по отдельности характеристики проводимости в области равновесной адсорбции и неравновесной ( необратимой) адсорбции. [7]
Весь участок изобары адсорбции до максимума кривой соответствует ложному равновесию: истинное равновесие здесь не достигается из-за малых скоростей хемосорбции. С дальнейшим ростом температуры равновесие хемосорбции - обратимой экзотермической реакции - смещается в сторону десорбции вещества с поверхности, что изображается правой нисходящей ветвью изобары адсорбции. Эта ветвь соответствует истинному равновесию. [8]
 |
Зависимость - &. U1 при адсорбции на графитированной термической саже к-алканов ( 1 и ди-к-алкилэфиров ( 2 от числа атомов углерода в их молекулах. [9] |
Выше 80 С изобары адсорбции хлоропрена проходят через минимум. Это указывает на вторичный процесс, протекающий вслед за молекулярной адсорбцией хлоропрена. [10]
На рис. VI-3 даны изобары адсорбции аммиака на древесном угле. [11]
На рис. 9 приведена изобара адсорбции СО на приготовленной нами ZnO. При низких температурах хемосорбция быстро уменьшается, обнаруживая минимум около 150; выше этой температуры адсорбированное количество несколько возрастает. Второй тип хемосорбции связан с гистерезисом и осуществляется в том температурном интервале, в котором легко обнаруживается кислородный обмен. [12]
 |
Соотношения между теплотой адсорбции и степенью покрытия, отвечающие уравнениям изотерм адсорбции Лэнгмюра ( /, Темкина ( 2 и Фрейндлиха ( 5. [13] |
Особое значение имеют изотермы и изобары адсорбции. Они являются основой математического описания адсорбционных процессов. [14]
 |
Изобары адсорбции водорода на никеле. [15] |
Страницы: 1 2 3 4 5