Восстановление - радикал
Cтраница 1
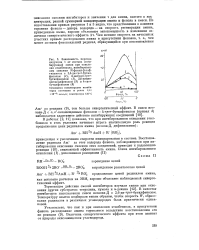 |
Зависимость периода индукции т от состава инги-бирующей смеси при окислении этилбензола, ингибирован-ном смесями N-фенил-р - наф-тиламипа с 2 6-ди-трег - бутил. [1] |
Восстановление радикала Am за счет водорода фенола, наблюдающееся при ин-гибировании окисления смесями этих соединений, приводит к подавлению реакции ( 10), снижающей эффективность амина. [2]
Восстановление радикала In - оксиперекисным радикалом было доказано следующим образом [89]: в циклогексанол, содержащий инициатор, в присутствии кислорода, когда оксиал-кильные радикалы быстро превращались в оксиперекисные, вводился тетрафенилгидразин. [3]
Вторая волна соответствует восстановлению радикала. В нейтральной среде непротонированная форма восстанавливается при том же потенциале, что и радикал. Из этого следует, что получение пинакона целесообразно проводить в кислых растворах. [4]
Наряду с этим происходит также восстановление радикалов с последующим раскрытием цикла. [5]
Это значение, видимо, относится к восстановлению радикала до аниона. [6]
Предположение, что восстановлению предшествует гомолитическое расщепление связи С-С и восстановление радикала, отпадает, так как спектры ЭПР показали, что в растворе свободные радикалы появляются лишь при высоких температурах и быстро исчезают при охлаждении. Гетеролитическое расщепление связи С-С в растворе ( с образованием соответствующего катиона и аниона без участия электронов) и последующее восстановление карбониевого катиона, подобно катиону трифенилметила [24], также не было доказано. Имеются данные и о полярографической активности роданидов. [7]
При переходе от водных растворов к растворам в органических растворителях потенциалы полуволн восстановления радикалов 2, 4, 8, 9 сдвигаются в область более отрицательных значений по мере ослабления протогенного характера растворителя в ряду: вода - 20 % - й этанол - этанол - бензол метанол ( 1: 1) - диметилфор-мамид. Влияние фонового электролита, а также природы заместителей в положении 4 пиперидинового цикла на электрохимическое восстановление нитроксильных радикалов Выражено значительно слабее, чем влияние растворителя. [8]
В присутствии других катализаторов, например никеля Рснея или палладия на угле, восстановление радикалов завершается образованием аминов. [9]
При высоких скоростях развертки потенциала с реакцией отщепления протона начинает конкурировать гетерогенный процесс восстановления радикала - RH, н на циклической вольт-амперограмме появляется обратный пик. Экспериментально определенные потенциалы восстановления радикала - RH находятся в хорошем соответствии с потенциалами, предсказанными на основании корреляции между Е и энергией орбитали, рассчитанной методом МОХ, если предполагать, что протонирование дианиона происходит по положению, для которого расчет методом МОХ дает наибольшую плотность заряда. Восстановление радикалов - RH, образующихся из альтернантных углеводородов, всегда протекает соучастием несвязывающей молекулярной орбитали, а экспериментальные значения потенциала, при котором происходит их восстановление, близки к - 1 1 В ( отн. [10]
Для того чтобы избежать нежелательной реакции восстановления свободного радикала, так же как в случае восстановления бензофенона, потенциал катода должен быть менее отрицательным, чем потенциал восстановления радикала. Используя электролиз с постоянным потенциалом, Аллен синтезировал многочисленные замещенные гликоли с высоким выходом. [11]
Таким образом, реакции окисления исходного изопропиль-ного радикала СН3 - СН-СН3 приводят к образованию СН3СНО, СН3ОН, С3Нв и продуктов окисления альдегидов СО или С02 и Н20 с восстановлением радикала С3Н7, начинающего новую цепь реакций. [12]
При взаимодействии радикалов цепи с молекулами замедлителя должны образовываться достаточно инертные радикалы, которые успеют рекомбинировать друг с другом раньше, чем войдут в реакцию с реагирующим веществом с восстановлением радикала цепи. [13]
Таким образом, реакции окисления исходного изопропиль-ного радикала СН3 - СН - СН3 приводят к образованию СН3СНО, СН3ОН, С3Н6 и продуктов окисления альдегидов СО или С02 и Н20 с восстановлением радикала С3Н7, начинающего новую цепь реакций. [14]
Это соединение представляет собой красноватую жидкость, перегоняющуюся без разложения и устойчивую к действию кислорода, воды и водной щелочи. Восстановление радикала приводит к образованию N-ди-отрет - бутилгидроксиламина, который при окислении воздухом быстро вновь превращается в радикал. [15]
Страницы: 1 2 3