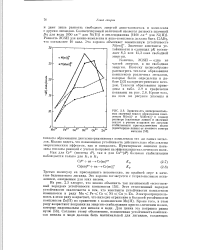
Акво-комплекс
Cтраница 1
Акво-комплексы Си2 и Ti3 имеют тетрагонально искаженную конфигурацию. [1]
Акво-комплексы Ga ( III) и In ( III) бесцветны, a TI ( III) слабожелтоватого цвета. [2]
Лабильность акво-комплексов, как правило, растет по мере пог нижения ионного потенциала, за исключением переходных металлов, где это явление зависит от конфигурации d - электронов. [3]
Скорость образования акво-комплексов можно повысить с помощью веществ, образующих комплексы с лигандом L, в результате чего связь М - L ослабляется. [4]
Скорость реакций акво-комплексов Ni ( ll) с октаэдрической конфигурацией также не зависит от природы лигандов. [5]
Но в акво-комплексах ион Pd ( H2O) имеет спин-спаренную конфигурацию и все комплексы платины и палладия диамагнитны. Коричневые расплывающиеся на воздухе соли, такие, как [ Pd ( H20) 4 ] ( С1О4) 2, можно получить при растворении палладия в азотной кислоте или PdO в хлорной кислоте. [6]
Но стоит лишь акво-комплексы обработать водой, ацетатом, аммиаком или щелочью, как они окрашиваются в темно-коричневый цвет и становятся крайне инертными. Подобное поведение наблюдается и для хрома ( III) и ряда других ионов ( ср. Необычайно прочные координационные связи между ионами и фиксированными группами смолы по сравнению с лабильной координацией дополнительных лигандов делают хелоновые смолы особенно пригодными для этого нового хроматографического метода. [7]
Замещение воды из акво-комплекса является обратной реакцией кислотного гидролиза, и иногда эту реакцию называют реакцией анации. [8]
Если молекулы воды в акво-комплексе замещаются каким-либо другим лигандом, то характер спектра обычно не изменяется, но полосы поглощения сдвигаются. Таким образом, величина Dq является как функцией лиганда, так и функцией центрального иона. [9]
Разность ЭСКП для амино-комплекса и акво-комплекса должна быть 12 / Dq, что составляет 10 ккал. [11]
Гидратацию катионов можно рассматривать как образование акво-комплексов, прочность которых определяется величинами констант нестойкости. Легкость, с которой ионы металлов образуют гидраты, возрастает с увеличением их заряда и уменьшением радиуса. Гидраты ионов щелочных металлов нестойки, щелочно-земельных более прочны. Например, гидратированный ион кальция, в основном определяющий жесткость природной воды, может быть представлен в виде октаэдра 1Са ( Н2О) в ] 2, в центре которого находится ион кальция, электростатически связанный с шестью молекулами воды, расположенными в его вершинах. [12]
Для элементов этой группы характерно образование акво-комплексов, особенно для циркония, гафния и тория. [13]
В такой схеме существует псевдоравновесие между акво-комплексом и пен-такоординироваиным интермедиатом. [14]
Они показывают, что внутренняя координационная сфера акво-комплексов этих ионов длительное время существует в виде стабильного образования. [15]
Страницы: 1 2 3 4