Анодное активирование
Cтраница 3
Это свидетельствует об обоснованности развитых в работе [4] представлений, согласно которым выделяющийся в условиях анодного активирования водород играет определенную роль в коррозионном растрескивании хромоникелевых сталей в хлоридных средах. Выявленные закономерности проявления отрицательного дифференц-эффекта с выделением водорода позволяют также рекомендовать его для использования в качестве критерия при оценке устойчивости хромоникелевых сталей к коррозионному растрескиванию. [31]
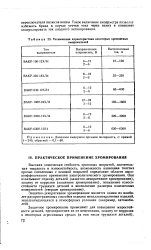 |
Техническая характеристика некоторых кремниевых выпрямителей. [32] |
Такое включение амперметра позволит избежать брака в случае утечки тока через ванну и позволяет контролировать ток анодного активирования. [33]
При осаждении хрома на детали из меди, медных сплавов или детали, имеющие медное покрытие, анодное активирование не проводят. Медь и медные сплавы активно растворяются в электролите хромирования. Чтобы исключить подтравливание и обеспечить прочное сцепление хромового покрытия с основным металлом, детали загружают в электролит под током. [34]
Интересно, что в метанольных растворах из-за недостатка воды и, следовательно, уменьшения степени пассивности, анодное активирование титана вызывается даже ионами NO3 -, которые обычно в водных растворах являются пассивато-рами. Питтинговая коррозия титана в органических средах может быть предотвращена, если концентрация воды будет превышать некоторое критическое значение. [35]
Интересно отметить, что в ыетанолъных растворах из-за недостатка воды и, следовательно, уменьшения степени пассивности анодное активирование титана вызывается даже ионами Я0 -, которые обычно в водных растворах являются пасси-ваторами. [36]
Интересно отметить, что в метанольных эастворах из-за недостатка воды и, следовательно, уменьшения: тепени пассивности анодное активирование титана вызывается хаже ионами N0 - которые обычно в водных растворах являются пассиваторами. [37]
При анодном активировании в хромировочной ванне электролит загрязняется железом, однако, как показала практика, накопление железа происходит очень медленно, поскольку анодное активирование при длительном износостойком хромировании производится относительно редко. Анодное активирование в хромовом электролите является очень важной операцией, так как от нее зависит сцепление хромового покрытия с основным металлом. При этой операции хромируемая поверхность полностью очищается бурно выделяющимся кислородом от остатков органических загрязнений. Слабым протравливанием с нее удаляют тонкие окисные пленки и поверхностный слой металла с искаженной структурой, обеспечивая наилучшие условия для надежного сцепления хрома со сталью. [38]
Полученные данные согласуются с результатами Хоймана и Хаука [13, 14], которые показали, что именно реакция окисления Мо02 до шестивалентного состояния определяет скорость анодного активирования этого металла, а не прямое окисление металлического молибдена до шестивалентного состояния. [39]
КР стали Х18Н10 в роданидных средах ( например, в производстве волокна нитрон) связано, как и в хло-ридных средах, с локальным анодным активированием. [40]
В статье показано, что ОСНОВНОЕ причиной коррозионного растрескивания аустенитных хроыоникелевнх сталей с различным содержанием хрома в растворах серной кислоты с добавками хлорида натрия является локальное анодное активирование пассивной поверхности. Увеличение содержания хрома в исследуемых сталях приводит к возрастанию времени до возникновения коррозионных трещин за счет роста устойчивости пассивного состояния. Для ускоренных испытании нержавеющих сталей аустенитного класса на восприимчивость к коррозионному растрескиванию рекомендуется потенциостатияеская выдержка нагруженных до 0 8 - 0 9 60 2 сталей в области неустойчивого пассивного состояния. [41]
Фокина, В. А. Тимонина, В. Ю. Васильева, С. Ш. Подольской показали, что коррозионное растрескивание металлов в нейтральных электролитах, по крайней мере в начальных стадиях, является следствием локального анодного активирования поверхности и ускоряется анодной поляризацией и полностью тормозится катодной поляризацией, причем с уменьшением кислотности среды расширяется область потенциалов, при которых возможно коррозионное растрескивание по этому механизму. [42]
Таким образом, предложенный механизм растворения алюминиевого протектора состоит из двух субстанций: а - хлоридного коррозионного разрушения и б - наводорожи-вания алюминиевого слоя катодно восстановленным водородом при анодном активировании. [43]
При анализе экспериментальных результатов представленных на рис. I и 2, обращает на себя внимание тот факт, что уже при анодном токе порядка нескольких мА / см2 процесс анодного активирования выходит на насыщение. Это существенно отличает процесс анодного активирования хромистых чугунов от анодного активирования коррозионностойких сталей. [44]
Перхлорат-ионы, способные при достаточно высокой концентрации подавлять ими же вызываемую активацию в области потенциалов от 0 8 до 1 4 в, совершенно не в состоянии воспрепятствовать другому процессу анодного активирования, который начинается при ф 1 4 в. Однако перепассивация приводит лишь к неболыпоТиу повышению скорости растворения пассивного металла. Это явление происходит, по-видимому, и при концентрациях перхлората 10 4 - 10 3 молъ / л, но прирост плотности тока, вызванный перепассивацией в этих условиях, вероятно, столь незначителен по сравнению с общей скоростью растворения, что обнаружить его на поляризационных кривых не удается. [45]
Страницы: 1 2 3 4