Активность - свободный радикал
Cтраница 3
В то же время свободные радикалы, образовавшиеся из мономеров, поляризованных вследствие сопряжения, всегда мало активны. Это объясняется тем, что активность свободного радикала обусловлена наличием неспаренного электрона. При сопряжении неспаренного электрона с другими связями электронное облако размывается и активность радикала уменьшается. Поэтому наиболее активные свободные радикалы образуются из мономеров, не активированных сопряжением. [31]
В то же время свободные радикалы, образовавшиеся из мономеров, поляризованных вследствие сопряжения, всегда мало активны. Это вызвано тем, что активность свободного радикала обусловлена наличием неспаренного электрона. При сопряжении неспаренного электрона с другими связями облако размывается и активность радикала уменьшается. [32]
Одним из важнейших факторов, влияющих на термоокислительную деструкцию полимера в масле, является химический состав масла, поскольку всегда протекают сопряженные процессы окисления углеводородов масла и полимера. При этом изменяется число и активность свободных радикалов, а следовательно, скорость и глубина окисления. [33]
В то же время свободные радикалы, образовавшиеся из мономеров, поляризованных вследствие сопряжения, всегда мало активны. Это объясняется тем, что активность свободного радикала обусловлена наличием неспаренного электрона. При сопряжении неспаренного электрона с другими связями электронное облако размывается, и активность радикала уменьшается. Поэтому наиболее активные свободные радикалы образуются из мономеров, не активированных сопряжением. [34]
Кинетическое поведение катионов определяется их активностью. Ряд активности карбкатионов совпадает с рядом активности соответствующих свободных радикалов - следствие индуктивного влияния заместителей. Чем больше положительный индуктивный эффект, тем меньше становится положительный заряд на валентно ненасыщенном атоме углерода катиона и тем меньше его реакционная способность. [35]
Преобладание процессов образования полимерных продуктов над процессом образования низкомолекулярных соединений при низких анодных плотностях тока и высоких концентрациях гало-генсодержащего мономера становится совершенно понятным, если учесть, что при низких плотностях тока на поверхности анода создаются незначительные концентрации радикалов, инициирующих реакцию полимеризации. В то же время при значениях потенциала анода, соответствующих низким плотностям тока, активность свободных радикалов не столь значительна, как при высоких плотностях тока. Все это создает условия для ухода свободных радикалов с поверхности электрода в раствор и встречи там с молекулами мономера. [36]
Для осуществления катионного механизма при радиационной полимеризации необходимо создать условия сохранения катионов М и стабилизации вторичных электронов, способных к их нейтрализации. Это достигается проведением полимеризации при низких температурах, когда продолжительность жизни ионов возрастает и активность свободных радикалов резко снижается. [37]
При достаточно высокой температуре энергия активации становится столь малой, что каждый или почти каждый удар газовой молекулы о поверхность углерода приводит к реакции. Это значит, что большая часть расположенных на поверхности атомов углерода имеет активность, аналогичную активности свободных радикалов. [38]
Более типичны случаи ослабления свободных радикалов за счет втягивания электрона в сопряженных системах. К числу последних прежде всего относятся радикалы аллилыюго типа, в которых смещающее влияние двойной пшзл на сопряженный с ней неспаренный электрон влечет за собой резкое падение активности свободного радикала. Те те соображения вполне применимы к объяснению причин, низкой активности бензилыгого свободного радикала. В согласии с высказанной точкой зрения о влиянии полярного фактора на реакционноспособность свободных радикалов находится также высокая активность таких радикалов, как фенил и атом водорода, для которых поляризация, подобно метальному радикалу, практически отсутствует. [39]
Как уже отмечалось, поляризованная молекула мономера легче реагирует со свободным радикалом. В то же время свободные радикалы, образовавшиеся из поляризованных молекул мономера, всегда менее активны, чем радикалы неполяризованных молекул. Активность свободного радикала определяется тем, насколько легко неспаренный электрон вступает во взаимодействие с п-связью двойной связи мономера. Делокализация электрона вследствие сопряжения уменьшает вероятность этой реакции, а следовательно, и активность радикала. [40]
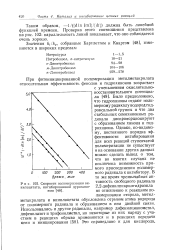 |
Скорости полимеризации винилацетата, ингибированной дурохино-ном. [41] |
Было предположено, что гидрохиноны отдают полимерному радикалу водород гид-роксильной группы и что два стабильных семихинонных радикала диспропорционируют с образованием хинона и гидрохинона. Однако, по-видимому, постоянного порядка эффективности ингибирования для всех реакций ступенчатой полимеризации не существует и на основании других данных можно сделать вывод о том, что во многих случаях не исключена возможность прямого присоединения полимерного радикала к ингибитору. В то же время чрезвычайная активность свободного радикала 2 2-дифенилпикрилгидразила по отношению к реакциям полимеризации стирола, метилметакрилата и винилацетата обусловлена отрывом атома водорода от полимерного радикала и образованием в нем двойной связи. [42]
Присутствие в молекуле мономера заместителей с положительным индуктивным эффектом также уменьшает реакционную способность радикала из-за частичного спаривания свободного электрона. Эффекты сопряжения больше влияют на активность радикала, чем на реакционную способность мономера. Поэтому скорость реакции роста цепи при радикальной полимеризации, по-видимому, зависит главным образом от активности свободного радикала. [43]
В реакциях жидкофазного окисления углеводородов ведущую роль играют перекисные радикалы RO. J, а скорость окисления определяется их активностью и концентрацией. За последнее время в работах [1-4], посвященных изучению реакций окисления, сформулированы некоторые причины изменения активности свободных радикалов под влиянием растворителей. Перекисные радикалы могут образовывать водородные связи с гидроксилсодержащими молекулами растворителя [4], вследствие чего их активность снижается. Ароматические углеводороды ( бензол и его производные) образуют с перекисными радикалами - комплексы [1,5], что снижает их активность. При окислении полярных соединений необходимо учитывать влияние диэлектрической постоянной на реакцию RO. С другой стороны, присутствие полярного растворителя увеличивает скорость распада гидроперекисей ( главных поставщиков свободных радикалов в реакциях жидкофазного окисления углеводородов) за счет неспецифической сольватации молекул гидроперекиси растворителем. В отдельных случаях существенную роль играет специфическая сольватация - ассоциация посредством водородных связей гидроперекиси между собой при их больших концентрациях или с электроноакцепторными соединениями ( например: гидроперекись третичного бутила-пиридин [6], гидроперекись изопропилбензола-нитробен-зол [7], что приводит к увеличению скорости распада, а следовательно, и к концентрации свободных радикалов. [44]
Страницы: 1 2 3