Активность - эфир
Cтраница 2
Изучение физиологической активности на растениях позволяет сделать некоторые выводы о зависимости активности эфиров дитиокарбаминовых кислот от их строения [230, 231], хотя дл. Я широких обобщений данных еще недостаточно. [16]
Добавление простых эфиров к системе TiJ4 - ( J-Bu) 3Al ( позволяющей получить полибугадиен с Содержанием - 90 % 1 4 - Ч с-звеньев, оставляя постоянным количество 1 2-звеньев), увеличивает содержание 1 4-гранс-звеньев симбатно количеству добавленного эфира. Активность эфиров уменьшается ъ ряду: ди-метиловый метилэтиловый диэтиловый дибутиловый, что совпадает с изменением склонности к комплексообразованию. [17]
Ярко выраженные электронодонор-ные свойства алкоксильных групп объясняют природу высокой активности простых виниловых эфиров. Активность випилалкиловых эфиров убывает в след, ряду заместителей: изопропил изобутил и-бутилэтил метил. Винилариловые эфиры не полимеризуются под действием нек-рых катализаторов К. [18]
Всходы проса и овсюга полностью уничтожаются при обработке 2р % - ным дустом диэтиленгликолевого эфира в дозе 14 кг / га. Изучена активность галоидарилоксиалкило-вых эфиров а а р-трихлорпропионовой кислоты, оказывающих гербицидное действие на сорняки, в частности гумай и канареечник, при послевсходовом опрыскивании. [19]
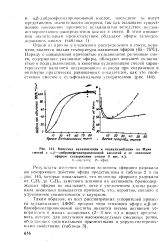 |
Кинетика вулканизации и подвулкани зации по Муни смесей с u f - дибромефенилпропионовой кислотой и ее этиловым эфиром ( содержание смолы 8 вес. ч.. [20] |
Результаты изучения влияния величины эфирного радикала на ускоряющее действие эфира представлены в таблице 2 и на рис. 145, которые показывают, что величина эфирного радикала от С. CgHig заметного влияния на активность бромсодер-жащих эфиров не оказывает, хотя с увеличением длины радикала несколько повышается прочность, что, вероятно, связано с улучшением совместимости с каучуком. [21]
Все ара-производные практически неактивны, активность орго-производных также значительно ниже активности исходного эфира. При наличии в мета-поло-жении фенильного остатка заместителей первого рода активность эфира повышается. Зависимость активности от строения арильного радикала и природы заместителей ( если их два и более) достаточно сложна, и четкие закономерности не выявлены. [22]
Все пара-производные практически неактивны, активность орго-производных также значительно ниже активности исходного эфира. При наличии в мета-положении фенильного остатка заместителей первого рода активность эфира повышается. Зависимость активности от строения арильного радикала и природы заместителей ( если их два и более) достаточно сложна, и четкие закономерности не выявлены. [23]
Наиболее высокой активностью обладают эфиры этих кислот, содержащие три-четыре атома углерода. Если число углеродных атомов в эфирном радикале превышает пять, активность эфира падает. [24]
Как показано выше, / V-алкил - и М М - диалкил-5 - алкилтиокарба-маты являются активными гербицидами, которые используются для борьбы со многими сорными растениями в различных культурах. Наиболее широкое применение в качестве гербицидов получили тиоловые эфиры тиокарбаминовой кислоты, гербицид-ная активность тионовых эфиров тиокарбаминовой кислоты существенно ниже, что обусловлено различиями их метаболизма в объектах окружающей среды. [25]
Как показано выше, / V-алкил - и А УУ-диалкил-З-алкилтиокарба-маты являются активными гербицидами, которые используются для борьбы со многими сорными растениями в различных культурах. Наиболее широкое применение в качестве гербицидов получили тиоловые эфиры тиокарбаминовой кислоты, гербицид-ная активность тионовых эфиров тиокарбаминовой кислоты существенно ниже, что обусловлено различиями их метаболизма в объектах окружающей среды. [26]
Активность алкиловых эфиров N-фенилкарбаминовой кислоты зависит от величины алкильного остатка и наличия заместителей как в фенильном, так и в алкильном остатках. Так, наиболее высокой активностью обладают алкил - М - фенил - и алкил - М - л-хлор-фенилкарбаматы, алкильные остатки которых содержат три-четыре атома углерода; при числе атомов углерода больше пяти активность эфира уменьшается. [27]
Таким образом, кажется возможным, что молекула действует per se независимо от какого бы то ни было посте, пенного разложения. Далее, можно предположить, что если токсическое действие этих двух 2-фторэтиловых эфиров действительно зависит в первую очередь от всей молекулы ( в отличие от продуктов гидролиза), то такое действие может быть приписано конечным атомам фтора в молекуле; если это так, то должно 61ть какое-то оптимальное расстояние от атомов фтора для того, чтобы молекула оказывала максимальное токсическое действие. Большое значение для различия активности этиловых и 2-фторэтиловых эфиров имеет длина цепи: чем цепь короче, тем активность выше. Это различие очень мало у фторгептанкарбоксилата, а у чонан-карбоксилатов оно совершенно исчезает. [28]
В реакцию с фенолами вступают многие эфиры р-кетшокислот, имеющие в у-положснии вместо метильных групп иные радикалы. Эфир бутирилуксусной кислоты [35], который можно рассматривать как эфир у-этилацетоуксуеной кислоты, и эфир у-фенил - - ацетоуксуеной кислоты [80, 81] реагируют С резорцином, орсиноы, пирогаллолом, флороглюцином и а-нафтолом, образуя производные соответственно 4-пропил - и 4-бснзилкумарина, но не реагируют с фенолом, J3 - нафтолом, гидрохиноном, л-крезолом, метиловым эфиром [ 3-резорциловой кислоты и резацетофсноном. Таким образом, заместители, находящиеся в т-положении, понижают активность эфиров [ 3-кетонокислот. [29]
 |
Продукты дегидратации этанола на алюмокалиевом сульфатном катализаторе при 275 С. [30] |
Страницы: 1 2 3