Относительная каталитическая активность
Cтраница 2
Сравнительное изучение каталитических свойств различных металлоферментов в начале было главным образом ограничено оценкой их относительной каталитической активности. Однако детальное изучение катализа и связывания лиганда для серии металлоферментов может пролить свет на роль иона металла, если при отсутствии каталитической активности сохраняется связывание металла. [16]
Тогда можно, проводя распад в слое, по изотопному составу углерода в продуктах разложения установить, какова относительная каталитическая активность разных участков. Имеются основания надеяться, что изотопный метод принесет ценные результаты в изучении механизма каталитических процессов и природы активной поверхности. [17]
Для определенного круга реакций можно теоретически вывести термодинамический критерий оптимального катализатора, с его помощью ориентировочно оценить ряд относительной каталитической активности и выделить таким путем вещества, активность которых целесообразно измерять на опыте в первую очередь. Если имеется возможность конкретизировать природу лимитирующей стадии ряда сходных процессов, протекающих на данном катализаторе, то, сопоставляя теплоты этих стадий, можно примерно оценить относительную реакционную способность различных веществ. EL ( для ряда сходных реакций на данном катализаторе) с использованием ограниченного числа экспериментальных кинетических данных позволяет методом интерполяции грубо оценивать абсолютную скорость для неизученных систем того же типа. Построение такого рода корреляционных зависимостей может служить также одним из методов отыскания рациональной классификации в катализе, поскольку оно позволяет выявлять однотипные системы. [18]
В табл. 42 представлены результаты расчета прочности связей в супероксидах благородных металлов и на основании этих данных оценена81 82 относительная каталитическая активность благородных металлов в процессе окисления этилена в окись этилена при 500 К. [19]
В настоящее время общепризнано, что первая стадия этой реакции имеет электронный характер, и это дает возможность исследовать относительную каталитическую активность различных окислов в зависимости от их электронной структуры. [20]
Методы приготовления окиси титана обсуждались также Бишо-фом и Эдкинсом [22], которые пришли к следующему выводу: свойства поверхности, влияющие на относительную каталитическую активность, очевидно, определяются не только размером и формой радикала, связанного с титаном при переходе соединения в твердое состояние, но также механизмом гидролиза и дегидратации исходного вещества. [21]
Теоретический анализ показывает [17], в согласии с опытом, что оптимальному катализатору процесса глубокого окисления любого веществ отвечают невысокие значения 7S ( порядка 15 - 25 ккал); этим объясняется отмеченное выше сходство в рядах относительной каталитической активности для окисления органических соединений весьма различного строения. [22]
Сравнение катализато - ров полизтиленполиамина и октоата олова при одинаковой их массовой концентрации в растворе ( кривые 1, 3) показывает, что усилие отслаивания существенно снижается при применении октоата олова, что связано, очевидно, с повышенной относительной каталитической активностью этого соединения. [24]
Рассмотрим теперь некоторые примеры специфических отклонений от соотношения Бренстеда, в особенности те, для которых можно дать разумную молекулярную интерпретацию. Значительное внимание было уделено исследованию относительной каталитической активности и силы оснований первичных, вторичных и третичных аминов. Прекрасная корреляция между каталитической активностью оснований по отношению к реакции разложения нитрамида в водном растворе [31] и величинами их рД была установлена для ограниченного ряда замещенных в кольце анилинов. Аналогичные корреляции были найдены для той же самой реакции в изо-пентаноле [32] и в ж-крезоле [33], причем в качестве характеристики силы основания использовались значения р / С в водном растворе. [25]
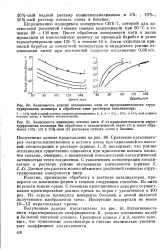
В ряде случаев существенное изменение каталитической активности катализаторов наступает в результате весьма незначительного изменения содержания промотора. На рис. 36 приводится зависимость относительной каталитической активности палладия в реакциях разложения перекиси водорода 2Н2О2 - 2Н2О О2 ( /) и гидрирования этилена С2Н4 Н2 - С2Нв ( 2) от концентрации фосфора в объеме палладия. Как видно из рисунка, каталитическая активность катализатора резко изменяется с изменением концентрации промотора. [26]
Все же в представлениях о механизме катализа достигнуты большие успехи, позволившие выдвинуть некоторые общие принципы выбора катализаторов для различных типов реакций. На рис. 2.17 представлены результаты изучения относительной каталитической активности металлов четвертого - шестого периодов в реакции разложения аммиака. Представленный график показывает периодичность изменения каталитических свойств с максимумами активности у железа и его аналогов у рутения и осмия. [27]
Было показано, что существует приблизительный параллелизм между каталитической активностью окислов в реакции Н2 с 02 и теплотой образования окиси металла, рассчитанной на 1 г-атом кислорода. Иначе говоря, можно считать, что относительная каталитическая активность связана с относительной восстанавливаемостью соответствующего окисла. Последние сделали допущение об образовании низших окислов и получили обычную вулканообразную кривую, выражающую соотношение между каталитической активностью и энергией взаимодействия промежуточных продуктов реакции с поверхностью. [28]
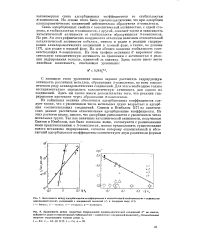
Связь адсорбционных свойств с каталитической активностью, с одной стороны, и стабильностью я-комплексов, с другой, означает также и зависимость каталитической активности от стабильности образующихся я-комплексов. На рис. 8 в логарифмических координатах отложены величины относительной каталитической активности кобальта, никеля и родия в реакции гидрирования алкилароматических соединений в газовой фазе, а также, по данным [17], для родия в жидкой фазе. На оси абсцисс нанесена стабильность соответствующих я-комплексов. На этом графике величины kr выражают относительную каталитическую активность по сравнению с активностью в реакции гидрирования толуола, принятой за единицу. [30]
Страницы: 1 2 3